Помогите не знаю как понять помогают антибиотики или нет!
Нечего бояться: 10 мифов об антибиотиках, которые мешают лечению
Без антибиотиков невозможно представить себе современную медицину, а сами они ушли далеко вперёд от пенициллина, изобретённого почти сто лет назад.
Сегодня они способны бороться с супербактериями и лечить неосложнённый аппендицит, а получить их пытаются из самых неожиданных источников — будь то почва, муравейник, кровь комодского варана или молоко утконоса.
Бесконечный поиск связан с тем, что чем дольше человечество использует антибиотики, тем выше вероятность устойчивости бактерий к ним — то есть риск того, что потребуются новые средства. А если учесть, что антибиотиками, сами того не подозревая, лечились даже неандертальцы, становится понятно, что у бактерий было достаточно времени, чтобы приспособиться.
Не менее важная, чем бактериальная резистентность, проблема — мы слишком мало знаем об антибиотиках.
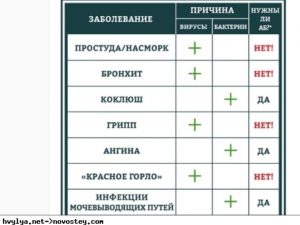
Точнее, знаний о них уже предостаточно, но почему-то мы продолжаем верить в мифы: многие люди до сих пор уверены, что антибиотики способны вылечить грипп, хотя вирусные инфекции ими лечить бесполезно. Это лишь одно из распространённых заблуждений.
Мы собрали ещё десять, которые помогут понять, что такое антибиотики и почему они скорее безопасны, чем опасны, но злоупотреблять ими всё равно не следует.
Антибиотики надо принимать с пробиотиками
Антибиотики уничтожают бактерии, а пробиотики восстанавливают кишечную микрофлору — звучит логично. Однако на самом деле ни дисбактериоза, ни молочницы антибиотики в подавляющем большинстве случаев не вызывают. Безусловно, небольшой риск сохраняется, однако обычно единственное, чем человеку грозит курс антибиотиков, — кратковременная диарея.
В отношении пробиотиков, если не брать в расчёт коммерческие исследования, врачи настроены скептически: необходимы дальнейшие исследования, чтобы понять, какие штаммы бактерий наиболее полезны и в каких дозах. Эксперты клиники Мейо уверены, что лучший способ привести кишечник в порядок — обильное питьё и выбор более мягкой в сравнении с обычным рационом пищи, а также сокращение объёма клетчатки.
Антибиотики всегда нужно пить курсом
Все мы не раз слышали, что курс антибиотиков обязательно нужно закончить — однако исследователи не уверены, что это так уж необходимо, если вам стало лучше.
Согласно недавним данным, досрочное прекращение антибиотикотерапии не способствует выработке устойчивости к ним, а вот более длительный, чем нужно, приём как раз повышает такой риск.
К тому же в целях удобства пациента новые средства стараются создавать так, чтобы их не нужно было принимать долго — и существуют даже антибиотики для однократного приёма.Впрочем, есть ряд заболеваний (наиболее очевидный пример — туберкулёз), при которых отказ от препарата в середине курса может привести к серьёзным последствиям. Эксперты говорят, что идеальная длина курса лечения пока не определена — она варьирует у разных людей и зависит в том числе от того, какие антибиотики применялись у человека в прошлом.
Нужно всегда делать тест на чувствительность
Такие анализы действительно помогают избежать многих проблем и назначить антибиотик, который будет работать именно так и с той скоростью, как хотелось бы врачу. Но во многих случаях врачебный алгоритм включает сначала назначение препарата широкого спектра действия, воздействующего на разные типы бактерий, включая наиболее вероятные при данном заболевании.
Только потом, в случае необходимости, назначается другой антибиотик, направленный на решение более узкой проблемы. При этом результаты исследований показывают, что антибиотики первого типа могут быть как минимум настолько же эффективны.
Антибиотики — безусловное зло для детей и беременных
Исследователи считают, что беременным женщинам стоит применять антибиотики с осторожностью. Что, впрочем, не означает, что они запрещены — важно лишь задуматься об их целесообразности в каждом конкретном случае. Антибиотики не опасны, но только если они принимаются по показаниям и в правильном режиме.
Недавно Всемирная организация здравоохранения обновила перечень основных лекарственных средств, разделив антибиотики на рекомендуемые, контролируемые и запасные — это важно именно для назначения «правильных» антибиотиков в каждом отдельно взятом случае.
Уколы лучше, чем таблетки
Пару десятилетий назад в больницах чаще использовали инъекционные, а не пероральные антибиотики.
Это было вполне оправданно, поскольку в арсенале врачей оказывались несовершенные препараты, а их выбор был довольно мал.
Биологическая доступность (то есть то, сколько препарата действительно поступало в кровь) тогда была выше для инъекционных форм (около 80 %, а для таблеток она составляла 40–60 %).
С тех пор в мире антибиотиков изменилось многое: они стали совершеннее, «научились» быстрее работать, а таблетки наконец смогли похвастаться биодоступностью в 90–95 % — это сделало внутримышечные уколы пережитком прошлого, особенно учитывая их болезненность; при внутривенном введении лекарство действительно подействует быстрее, но это нужно довольно редко. Антибиотики в таблетках проще в применении и значительно безопаснее. Правда, некоторые препараты пока нельзя заключить в таблетированную форму — они будут просто перевариваться ферментами в желудке.
Антибиотики можно применять для профилактики
Антибиотикопрофилактика используется для снижения риска инфекций, связанных с открытыми переломами и ранами, в том числе после операций, и в таких случаях она вполне оправданна. Но нередко под профилактикой антибиотиками подразумевается предотвращение инфекций в бытовых ситуациях — например, когда человек отправляется в отпуск в незнакомую страну и хочет, чтобы всё прошло гладко.
Речь в первую очередь идёт о кишечном расстройстве, известном как диарея путешественника и возникающем на фоне смены системы питания или климатической зоны.
Однако врачи по всему миру сходятся во мнении, что подобная профилактика — излишество.Правильнее и безопаснее с осторожностью относиться к выбору воды и пищи и, как вариант, попросить врача рекомендовать антибиотик на случай, если проблема всё-таки возникнет.
Резистентность возникает только из-за постоянного приёма антибиотиков
Широкое применение антибиотиков ускорило темпы, с которыми бактерии становятся устойчивыми к ним. Но думать, что только регулярный и неконтролируемый приём антибиотиков может привести к резистентности, неправильно.
Учёные установили, что виноваты могут быть гены антибиотикорезистентности, которые наделяют бактерии возможностью разрушать антибиотики класса карбапенемов — одни из главных средств против крайне опасных супербактерий.
Не так давно выяснилось, что некоторые бактерии в борьбе за территорию уничтожают другие микробы, «подбирая» остатки их ДНК, в которых могут содержаться гены устойчивости к антибиотикам, — и это усложняет задачу.
На данный момент перспективным вариантом решения проблемы кажется тщательное изучение плазмид — молекул, переносящих генетическую информацию — и разработка средств, которые помешали бы генам резистентности прикрепляться к этим плазмидам.
Любой антибиотик лучше,
чем ничего
Cуществуют ли универсальные антибиотики, которые в любом случае помогут? Ответ однозначный: нет. Существуют препараты широкого спектра действия, но даже их всегда назначают с учётом того, какой тип бактерий наиболее вероятен у пациента. Так что позиция «допью вот этот антибиотик, чтобы не покупать прописанный врачом» не работает.
По оценкам экспертов, около 50 % антибиотиков по всему миру приобретается без рецепта.
И в этом нет ничего хорошего: помимо всеобщей озабоченности растущим количеством устойчивых к антибиотикам бактерий, есть риск промахнуться если не с типом лекарства, то с его дозировкой или сочетаемостью с другими препаратами, требующими постоянного приёма.К тому же использование антибиотиков для борьбы со слабыми бактериальными инфекциями, такими как фарингит или бронхит, чаще всего не требуется, так как наша иммунная система способна справиться с этим самостоятельно.
Антибиотики в мясе — угроза здоровью
Начнём с того, что антибиотики в качестве стимуляторов роста или для лечения инфекций у животных используются не бесконтрольно — и постоянно ведутся исследования на эту тему. И пока ни одно из них не позволило обоснованно говорить о вреде такого применения для людей — другое дело, что количество красного мяса в рационе лучше ограничить по другим причинам.
Стоит иметь в виду, что даже в органическом, натуральном или биодинамическом фермерстве животных лечат антибиотиками, если это необходимо. Хотя, справедливости ради, недавно ВОЗ попросила фермеров не делать этого без особой надобности.
Антибиотики несовместимы с алкоголем
Большинство наиболее часто назначаемых антибиотиков вполне совместимы с алкоголем. Во всяком случае, один-два бокала вина не повод прерывать курс или думать, что антибиотики перестали действовать и их приём нужно начинать сначала.
Говорят, что совмещать алкоголь с антибиотиками запретили во времена Второй мировой войны. Тогда производство лекарства не было массовым и его использовали многократно — у пациентов собирали мочу, из которой затем получали новый пенициллин.
Пиво, которое позволяли себе солдаты, увеличивало объём мочи, и обрабатывать её становилось сложнее.
Есть и исключения: метронидазол, тинидазол, триметоприм, линезолид и некоторые другие антибиотики не следует смешивать с алкоголем, чтобы избежать неприятных побочных эффектов. И не стоит злоупотреблять алкоголем во время курса антибиотиков — он дополнительно ослабляет организм, что не способствует борьбе с инфекцией.
Фотографии: Mara Zemgaliete — stock.adobe.com (1, 2, 3)
Антибиотики перестали помогать. Почему так происходит и что делать?
Дина Ли специально для Informburo.kz
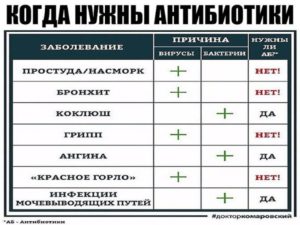
Мы поговорили с Анной Фарленковой, Директором отдела розничных продаж рецептурных препаратов компании SANTO, чтобы разобраться, почему антибиотики не лечат простуду, отчего со временем лекарства перестают помогать и как выстроить лечение правильно.
Что лечат антибиотиками?
Бактериальные инфекции. Именно поэтому в борьбе с вирусами, гриппом и простудой они бесполезны.
При этом важно понимать, что антибиотик антибиотику рознь, и нет универсальной таблетки, которая уничтожала бы любые бактерии.
Чтобы антибиотик сработал, бактерия должна быть чувствительной именно к этому препарату. Cуществуют и антибиотики широкого спектра действия: те, что направлены на борьбу с целым рядом бактерий.
Почему к приёму антибиотиков важно подходить рационально?
Со временем бактерии эволюционируют, адаптируются и становятся сильнее. Битва обычного пенициллина с такой “продвинутой” бактерией напоминает бой боксёра-любителя с мировым чемпионом: исход предрешён. Устойчивость бактерии к антибиотику называют резистентностью.
К сожалению, мы сами ускоряем выработку резистентности, когда пьём антибиотики без назначения врача, лечим ими вирусные заболевания и увеличиваем дозы, надеясь на быстрый эффект. Нерациональный приём антибактериальных препаратов приводит к тому, что организм перестаёт бороться с инфекциями, и когда антибиотик действительно будет необходим, он может не сработать.
Бактерии становятся “умнее”, а что насчёт антибиотиков?
Угнаться за бактериями непросто. К примеру, антибиотик тетрациклин появился в 1950 году, а первые бактерии с устойчивостью к нему – в 1959. Метициллин – в 1960 году, резистентные бактерии – в 1962. Ванкомицин открыли в 1972 году, а устойчивые бактерии появились в 1988.
Даптомицин появился в 2003, первые признаки устойчивости к нему – в 2004. В США в 80-х годах появилось около 18 новых антибиотиков, 10 лет спустя – около 12, в начале нулевых – четыре, а в 2010–2014 – всего один.
Кроме того, создание новых лекарств – процесс трудоёмкий и затратный.
Открыто пять поколений разных групп антибиотиков. Чем “старше” антибиотик, тем выше резистентность к нему. Но нельзя сказать, что препараты первого поколения объективно хуже, чем препараты пятого поколения. Поколения отличаются не по эффективности, а по спектру и принципу действия, поэтому сравнивать их бессмысленно – это разные лекарства, которыми лечат разные заболевания.
Проверенный антибиотик перестал помогать. Значит, у меня выработалась резистентность?
Маловероятно, но не обязательно. Чаще всего так случается, если вместо врача вы обратились за помощью к интернету, аптекарю, знакомым, или вспомнили прошлое. Это одна из самых распространённых ошибок: то, что раньше это лекарство при схожих симптомах дало эффект, не значит, что оно поможет снова.
Тем более, не стоит ждать скорого выздоровления, если препарат вам посоветовали друзья в социальных сетях. Только врач может поставить правильный диагноз, определить, с какой бактерией борется организм, и как ему эффективнее помочь.
Если же у вас в самом деле выработалась устойчивость к определённому антибиотику, специалист поможет подобрать другое лекарство.
Назначенного врачом препарата не оказалось в аптеке. Фармацевт посоветовал другой антибиотик. Можно ли заменить лекарство?
Аптекарь не знает вашей истории болезни, не видел анализов и не так компетентен, как врач.
К тому же, есть вероятность, что он преследует личную выгоду: старается продать лекарства, у которых истекает срок годности или у аптеки подписан договор с определённым поставщиком.
Это не значит, что любая рекомендация фармацевта направлена против вас, но рисковать здоровьем, заменяя антибиотик на аналоги, не стоит. Перед любой заменой лекарства нужно проконсультироваться с врачом.
Принимаю лекарство уже 2 дня, а эффекта нет. Как быть?
В целом, есть инфекции и препараты — когда курс может быть 1 таблетка (в основном урология) и есть зоонозы, которые перекрёстно лечатся до 14-21 дня . В среднем, курс приема антибиотика составляет 5-10 дней.
Важно принимать лекарство в соответствии с назначением врача. В любом случае, первичные симптомы болезни должны пройти в первые пару дней приёма препарата. Если этого не произошло, скорее всего, дело в резистентности микроорганизмов, и лекарство придётся менять.
Обязательно сообщите об этом врачу – он скорректирует схему лечения.
https://www.youtube.com/watch?v=-ZjCxL8ByM0
Отсутствие эффекта от приёма антибиотика особенно опасно, если вы пьёте лекарство не по назначению врача. Болезнь всё это время прогрессирует.
Можно ли сочетать антибиотики с другими лекарствами?
Да. Например, иногда врач может назначить сразу два антибиотика, чтобы убить основного и вторичного возбудителей, или в случае тяжелых инфекций, например, менингококковой инфекции, или в случае тяжелого состояния пациента.
С другими препаратами антибактериальную терапию тоже можно сочетать без проблем. Главное выдерживать интервалы: 1,5-2 часа между приёмом лекарств. Тогда оба препарата подействуют так, как должны.
Кроме того, антибиотики часто советуют принимать в комплексе с пробиотиками, чтобы поддержать ослабленный организм и кишечную микрофлору.
В казахстане производят антибиотики?
Производство антибиотиков на внутреннем рынке – вопрос государственной безопасности. Это сложнее, чем выпуск других препаратов. Например, компания SANTO стала первым фармацевтическим производителем в Казахстане, который производит антибактериальные препараты, соответствующие стандартам GMP.
Уже несколько лет в Шымкенте на заводе SANTO выпускаются антибиотики ряда пенемы/мицины и цефтриаксоны. В рамках долгосрочных договоров с государством компания SANTO является главным поставщиком антибактериальных средств по каналу гарантированного объёма бесплатной медицинской помощи.
в тексте, выделите ее мышью и нажмите Ctrl+Enter
Вам назначили антибиотики. Как узнать, что их выписали правильно

В эру до появления антибиотиков смерть от бактериальных инфекций была обычным делом. Даже самые легкие на первый взгляд болезни могли в считанные дни привести к смерти. Сегодня антибиотики могут вас спасти. Обычно с помощью них лечат бактериальные инфекции в легких, мочевыводящих путях, глазах, горле, на коже и в кишечнике.
Но далеко не все бактериальные инфекции нужно лечить антибиотиками, иногда инфекции проходят сами собой, без лечения. И конечно антибиотиками не лечат вирусные инфекции, такие как простуда и ОРВИ, или грибковые инфекции, такие как опоясывающий лишай или молочница.
Антибиотики нельзя считать универсальным методом лечения: не все антибиотики убивают все типы бактерий.
Как понять, какой тип бактерий вызывает инфекцию?
Если врач подозревает у вас серьезную бактериальную инфекцию, он берет вашу кровь или мочу на анализ, чтобы отправить в лабораторию. В лаборатории выявляются и идентифицируются бактерии, вызывающие инфекцию.
Есть генотипические методы для идентификации бактерий. Они основаны на определении гомологии ДНК искомого микроорганизма в исследуемом материале и являются быстрыми и высокочувствительными.
И есть другие методы, применяемые для культивирования и выделения бактерий из образца. Тесты в данном случае могут занять от одного до четырех дней.
Как подобрать антибиотик?
Если лечение антибиотиками необходимо, обнаруженные бактерии могут быть использованы, чтобы подобрать правильный антибиотик. Это так называемый тест на определение чувствительности отдельных групп бактерий к антибактериальным препаратам.
Эти тесты могут быть проведены на основе ДНК (генотипический метод) или путем определения чувствительности бактерий к антибиотикам (фенотипические методы).
Генотипические тесты, как правило, показывают какие антибиотики не сработают при лечении, то есть какие антибиотики можно исключить.
При фенотипических тестах бактерию заново выращивают, чтобы увидеть какой из антибиотиков остановит ее рост.
Почему иногда антибиотик назначается до результатов анализов?
Какие бы тесты не проводились, результаты могут быть недоступны в течение нескольких дней. Тем временем ваш врач, вероятно, уже назначит вам антибиотик, который скорее всего будет эффективным. Это называется эмпирической терапией — лучший вариант, пока врач ждет результаты теста.
Эмпирический выбор антибиотиков основывается на опыте врача, а также клинических рекомендациях, разработанных на основе фактических данных о типе инфекции, данных наблюдений в лаборатории за типами бактерий, обычно вызывающих эту инфекцию и чувствительности бактерий к антибиотикам.
Результаты анализов либо подтвердят первоначальный выбор врача, либо повлияют на его решение назначить другой антибиотик.
Возьмем, к примеру, инфекции мочевыводящих путей. Большинство из них вызываются кишечной палочкой и существуют антибиотики, которые хорошо лечат эту инфекцию. Данные тысяч тестов на кишечную палочку помогают врачу подобрать для вас эмпирический антибиотик и дать клинические рекомендации.Врач уверенно назначает антибиотик пока вы ждете результатов анализа мочи. И вы либо поправитесь, либо вернетесь к врачу, когда результаты анализов будут готовы для более точного подбора антибиотика.
Почему так важно подобрать антибиотик правильно?
Конечно, каждый человек хочет принимать тот антибиотик, который эффективно вылечит инфекцию. Но что плохого в приеме антибиотика, который делает свою работу слишком хорошо или, наоборот, малоэффективен?
Слишком сильные антибиотики не только убьют инфекцию, но и другие полезные бактерии, нарушив вашу кишечную микрофлору и, возможно, вызовут другие побочные эффекты.
С другой стороны, слабый антибиотик не только не сможет адекватно вылечить инфекцию, но вызовет побочные эффекты и нарушит вашу кишечную микрофлору.
Также чрезмерное или неэффективное использование антибиотиков способствует развитию устойчивости к ним бактерий, поэтому важно минимизировать и оптимизировать целевое использование антибиотиков.
Антибиотик может назначать только врач! Ни в коем случае не покупайте их самостоятельно без консультации со специалистом.
Правильно подобрать антибиотик непросто, хотя часто решение о его приеме нужно принимать до того, как появятся дополнительные доказательства. Однако после получения результатов анализов, лечение антибиотиками может быть уточнено, изменено или даже прекращено.
Перевод Марии Строгановой
Не помогают антибиотики: причины, правила приема и мнения врачей

Среди множества препаратов, которые поставляет современному человеку фармацевтический рынок, самыми действенными лекарствами против воспалительных процессов являются антибиотики. Но бывают случаи, когда назначенный специалистом препарат этой группы отказывается помогать в борьбе с болезнью. Что делать, если антибиотики не помогают? В статье вы найдете ответ на этот серьезный вопрос.
Что такое антибиотики?
Антибиотики в современной медицине представляют собой обширный спектр препаратов с противомикробным действием.
Эти лекарственные вещества можно классифицировать по составу, по спектру действия, по терапевтическим свойствам и побочным эффектам. Также существуют антибактериальные препараты широкого спектра действия.
Стоит отметить, что антибиотики известны не только своими терапевтическими свойствами, но и обширным списком побочных эффектов. При длительном использовании они пагубно сказываются на организме, поэтому их нельзя принимать без назначения лечащего врача.
Также стоит отметить, что простой обыватель не в состоянии поставить себе правильный диагноз, а при некоторых заболеваниях (вроде гриппа) антибиотики не помогают. Но существуют и другие причины, по которым возможно существование такой проблемы. Почему не помогают антибиотики, и что делать в случае этого?Иногда случается такое, что после прописанного врачом курса лечения, куда входили препараты антибактериальной группы, пациент не чувствует улучшения, что указывает на то, что инфекционное заболевание того или иного рода все еще не побеждено. Зачастую то, что антибиотики не помогают, может быть связано с невосприимчивостью организма больного к такого рода препаратам.
Как правило, такое случается у пациентов, которые в детстве имели некоторые инфекционные заболевания, например, ангину, в хронической стадии. На фоне этого ребенок часто болел, а врач прописывал антибиотики.
За многие годы микрофлора организма познакомилась со многими антибиотиками и перестала быть к ним восприимчива. То есть произошло привыкание.
В таком случае, если назначенные антибиотики не помогают, врач вынужден прописать более сильные вещества.
Также плохая восприимчивость формируется в случае неправильного курса антибактериальных препаратов. Поэтому к назначениям врача стоит относиться серьезно и пропивать препараты, строго соблюдая инструкцию.
При кашле
Перед тем, как говорить о лечении антибактериальными средствами, стоит отметить, что кашель — это не заболевание, а всего лишь его симптом. В зависимости от того, какой природы кашель — вирусной или бактериальной — лечащий врач выбирает, назначать антибиотики или нет. Как показывают опросы, многие люди после того, как обнаруживают у себя этот симптом, начинают принимать антибиотики.
Во-первых, частый прием такого препарата может пагубно сказаться на здоровье. Во-вторых, если кашель имеет вирусную природу, в таком случае антибиотики не помогают.
Стоит помнить, что принимать антибактериальные препараты стоит только в случае назначения врачом и наличии такого диагноза как:
- Воспаление легких.
- Туберкулез.
- Ангина.
- Коклюш.
Когда антибиотики не помогают, кашель вызван либо вирусной инфекцией, либо является аллергической реакцией на что-либо.
При температуре
Антибиотики не показаны к применению в случае повышения температуры, если этот симптом не является следствием воспалительного процесса, происходящего в организме пациента. При обычном ОРВИ назначается лечение с отсутствием таких сильных препаратов и соблюдением постельного режима.
Однако существует и такое явление, когда курс медикаментов антибактериального действия был пропит по назначению врача после правильно поставленного диагноза, а температура не спадает.
Такое явление называется «температурный хвост». Оно заключается в том, что после исчезновения воспалительного процесса организм продолжает поддерживать высокую температуру.
Это не означает, что антибиотики не помогают.
Такое явление никак не сказывается на самочувствии больного. Он не ощущает сопутствующих симптомов в виде головной боли, ломоты в теле и слабости. Но «температурный хвост» может означать начало нового воспалительного процесса, поэтому необходимо следить за состоянием больного.Также повышенная температура может быть связана с тем, что препарат подобран неправильно, или с тем, что курс лечения пациента не соответствует рекомендациям врача и инструкции. Таким образом, при температуре антибиотики не помогают, если не соблюдается правильное лечение, и если отсутствует воспалительный процесс.
Ребенку
Что делать, если ребенку не помогают антибиотики? Такими вопросами заполнены многие форумы. Ребенок, хоть и отличается от взрослого человека развитием как иммунитета, так и всего организма в целом, но принципы на него действуют аналогичные. Почему не помогают антибиотики?
Потому, что лекарственный препарат подобран неправильно. В настоящее время люди стараются лечиться антибактериальными препаратами неоправданно часто, что приводит к снижению чувствительности и проблемам с организмом.
Несмотря на то, что антибиотики для детей имеют более маленькие дозы, тем не менее, они остаются серьезным препаратом, и применять их при любой простуде не стоит, особенно, если не было соответствующего назначения от врача.
В противном случае может случиться такое, что антибиотики не помогут, когда ребенку потребуется реальное лечение воспалительного процесса.
Правила приема
Антибиотик — серьезный препарат, и перед тем, как принимать его, необходимо ознакомиться с определенным перечнем правил.
- Употреблять этот препарат только по назначению врача.
- Не изменять дозу принимаемого препарата самостоятельно. Многие люди, осведомленные о побочных действиях этого вещества, считают, что, уменьшив дозу, они сократят пагубное воздействие на организм. На самом деле, они дают болезнетворным бактериям шанс на выживание с сохраненной в геноме устойчивостью к данному препарату. По такому же принципу нельзя бросать прием антибиотиков, не пройдя полный курс, указанный врачом.
- Необходимо строго соблюдать время приема. Желательно помечать, когда была выпита последняя таблетка, и употреблять следующую через равный промежуток времени.
- Правильно запивать таблетку. Лучше всего это делать большим количеством воды. Нежелательно употреблять ее вместе с соками и газированными напитками.
- Соблюдать диету. Прием антибиотика — большой стресс для организма, поэтому необходимо поддержать его в этот период. Желательно на время лечения отказаться от жирного, соленого, острого. Лучше обогатить свой рацион пищей, содержащей клетчатку и витамины.
- Не менять антибактериальное средство без консультации врача.
Мнение врачей
В этом вопросе современные врачи выражают единое мнение — необдуманный прием данных препаратов в значительной степени сказывается на состоянии человека.
Это в дальнейшем может привести к серьезным проблемам, таким как невосприимчивость к антибиотикам, нарушение работы желудка и иммунодефицит.
Кроме того, антибиотики пагубно влияют на внутренние органы — такие, например, как печень, почки, желчный пузырь. Они склонны вызывать сильные аллергические реакции.
Поэтому при первых симптомах заболевания необходимо обратиться за помощью к врачу, а не принимать препараты самостоятельно. Применять антибиотики необходимо с осторожностью и только по назначению.
Перечень заболеваний
Представим некоторые заболевания, которые лечатся благодаря антибактериальным препаратам. К ним относятся:
- Бронхит.
- Синусит.
- Гнойный отит.
- Гайморит.
- Уретрит.
- Гастрит.
- Язва.
- Столбняк.
Помимо указанных заболеваний, существует еще множество, от которых спасают препараты данного спектра действия. Но стоит еще раз отметить, что подобные диагнозы человек не в состоянии поставить самостоятельно, а, значит, для этого необходимо обратиться к врачу.
Чем лечиться, когда антибиотики перестанут помогать

В начале ХХ века, еще до открытия антибиотиков, средняя продолжительность жизни даже в развитых странах составляла менее 50 лет. Главной причиной преждевременной смерти были бактериальные инфекции, такие как холера, дифтерия, туберкулез и сифилис.
После изобретения антибиотиков в здравоохранении все кардинально изменилось: врачи научились лечить прежде смертельные болезни, стало меньше госпитальных инфекций, стали возможными сложные операции и пересадка органов. Благодаря этому средняя продолжительность жизни в развитых странах увеличилась на десятки лет.
Сегодня эра антибиотиков, кажется, подходит к концу.
Все потому, что медики стали злоупотреблять препаратами: только в США в год выписывают более 250 млн курсов антибактериальных препаратов, или больше 800 назначений на 1000 жителей.
Пациенты тоже вносят свой вклад в развитие резистентности: они самостоятельно «назначают» себе антибиотики, когда они не нужны, не заканчивают курс, позволяя самым устойчивым бактериям выжить и размножиться.
Особенно сильно подрывают эффективность антибиотиков неоправданные назначения во время больничных инфекций: в таких ситуациях медики склонны выписывать антибактериальные препараты всем подряд, «для профилактики».
Но исследования показывают: когда врачи выписывают антибиотики только тем пациентам больницы, которым они реально нужны, это одновременно снижает количество устойчивых к лекарствам инфекций и уменьшает показатели смертности.Кроме прочих факторов, в растущей антибиотикорезистентности виновата сельскохозяйственная отрасль — в ней антибактериальные препараты используют до четырех раз чаще, чем в медицине.
Что произошло?
В итоге в природе появились особые микробы, которые не чувствительны к существующим антибиотикам. Среди таких бактерий — клебсиелла (Klebsiella pneumoniae), вызывающая пневмонию, и золотистый стафилококк (Staphylococcus aureus), который провоцирует гнойно-воспалительные заболевания.
Как формируется устойчивость бактерий? Допустим, человек не закончил курс антибиотиков.
Самые слабые микробы были уничтожены в первые несколько дней, но были и «счастливчики», которые выжили. Значит, что-то в их генах позволило им сопротивляться антибиотику.
Возможно, возникли какие-то приспособительные мутации, или эти бактерии изначально были не очень чувствительны к конкретному лекарству.
Выжившие бактерии каким-то образом — например, через немытые руки — попадают в окружающую среду. Там они, во-первых, могут вызвать инфекцию у другого человека — и ему уже не помогут те же самые антибиотики, ведь микробы научились им сопротивляться.
А во-вторых, резистентные бактерии начнут обмениваться генами устойчивости со своими собратьями и даже микробами других видов. Происходит это с помощью небольших молекул, плазмид, которые содержат генетическую информацию — бактерии передают их друг другу, распространяя гены резистентности.
Подобным образом микробы могут приобрести устойчивость к нескольким видам антибиотиков. Если человек заразился инфекцией, вызванной такими — полирезистентными — бактериями, врачам приходится применять новейшие, самые мощные лекарства с самым широким спектром действия (и массой побочных эффектов).
Сегодня такими антибиотиками «последней надежды» являются карбапенемы: когда они не помогают, дальше человека лечить уже нечем, и это практически смертный приговор. Уже появились бактерии, которые устойчивы и к карбапенемам (и они атакуют людей) — они способны вызывать масштабные больничные инфекции с уровнем смертности в 40-50%.
Depositphotos.com
Возврат к истокам: бактериофаги
Все описанное звучит пугающе. Ученые, конечно, давно забили тревогу по поводу антибиотикорезистентности — и начали разрабатывать альтернативные методы лечения бактериальных инфекций.
Одно из возможных решений — вернуться к препаратам, которые придумали еще 100 лет назад, до начала эры антибиотиков. Речь идет о бактериофагах.
На самом деле, не совсем верно говорить, что их «придумали» — скорее, ученые додумались использовать бактериофаги для борьбы с инфекциями. Ведь бактериофаги (или просто фаги) — это вирусы, которые живут в природе и регулируют численность бактерий.
Это самая многочисленная группа живых существ на планете, тем не менее долгое время их важность недооценивали, а сами бактериофаги практически не изучали. С 1919 года было несколько успешных опытов по излечению бактериальных инфекций фагами, но после открытия антибиотиков эти вирусы забросили.Терапия бактериофагами прижилась лишь на территории бывшего СССР. Советские ученые лечили фагами послеоперационные, урологические, дерматологические, глазные, стоматологические инфекции, заболевания ЛОР-органов.
Об этом даже писали научные работы, но так как все они были на русском языке, мировое сообщество ученых не имело к ним доступа.
К тому же, качество исследований советских ученых вызывало сомнения у их иностранных коллег.
Сегодня, в связи с кризисом антибиотиков, исследователи возвращаются к бактериофагам и пытаются оценить их эффективность. Пока что ученые относятся к фагам со сдержанным оптимизмом.
Есть надежда, что они смогут дополнить или заменить антибиотики в борьбе с резистентными бактериями.
Однако прежде, чем врачи начнут широко применять фаги в клинической практике, ученые должны получше изучить механизм их действия и возможные побочные эффекты.
Альтернативные решения
Возврат к наработкам прошлого — не единственное направление в борьбе с антибиотикорезистентностью. Ученые пытаются найти новые «бреши» в защитной системе бактерий и изобрести революционные лекарства, направленные на них.
Одна из потенциальных мишеней — те самые плазмиды, с помощью которых микробы обмениваются генами. Исследователи разрабатывают препараты, способные уничтожить плазмиды с генами устойчивости — таким образом они надеются вернуть бактериям чувствительность к стандартным антибиотикам.
Микробы могут противостоять антибактериальной терапии с помощью специального молекулярного насоса, который буквально «выкачивает» антибиотик из клетки.
Еще одно перспективное направление в борьбе против резистентных бактерий — придумать лекарства, которые будут «отключать» подобный насос.Наконец, ученые пытаются препятствовать самому процессу развития устойчивости у микробов.
Оказалось, что перед тем, как стать резистентными к антибиотикам, бактерии приобретают толерантность — то есть способность «уснуть» и не погибнуть под воздействием лекарства.
После пробуждения такие микробы начинают стремительно эволюционировать, становясь устойчивыми к антибактериальным препаратам. Исследователи хотят найти способы предотвратить толерантность — а значит, и остановить развитие устойчивости к антибиотикам.
К сожалению, эти и другие альтернативные методы лечения бактериальных инфекций пока лишь на стадии разработки.
Ученые надеются, что они смогут изобрести новые эффективные препараты против бактерий раньше, чем терапия антибиотиками полностью исчерпает себя.
А пока исследователи ищут решение проблемы резистентности, все, что вы можете сделать, — это не принимать антибиотики без острой необходимости, а в случае назначения — тщательно следовать указаниям врача и всегда допивать курс до конца.
Подробно о том, как принимать антибиотики, читайте здесь.
Обнаружили ошибку? Выделите ее и нажмите Ctrl+Enter.
Как работают антибиотики: когда они эффективны и бесполезны

Некоторые глотают антибиотики при малейшем насморке, другие категорически отказываются принимать их даже при жестокой пневмонии, считая их жутко вредными. И тот и другой подход абсолютно неверен.
Антибиотики действительно помогают справиться со многими тяжелыми инфекциями, но только в том случае, если принимать их правильно.
Чтобы понимать, в каком случае препарат подействует, а в каком окажется абсолютно бесполезным и даже вредным, надо представлять себе, как работает антибиотик в организме человека.
Антибиотик – что это за лекарство?
Уже в самом названии этой группы препаратов заключен основной принцип их действия: анти – против; биотик – жизнь.
Антибиотики – вещества природного происхождения, которые обладают свойством уничтожать другие живые микроорганизмы или препятствовать их размножению. В природе антибиотики вырабатываются некоторыми микроорганизмами как продукты их жизнедеятельности.
В фармакологии используют антибиотики:
- природные – выращивают микроорганизмы на питательных средах;
- полусинтетические – добавляют к природным другие вещества для улучшения их свойств;
- синтетические – получают полностью химическим синтезом.
Строго говоря, последние относят не к антибиотикам, а к антимикробным препаратам, но в быту мы тоже называем их антибиотиками.
Как работают антибиотики?
Если говорить простым языком, то действуют антибиотики двумя путями.
- Уничтожают микроорганизмы, в этом случае они называются бактерицидными. Как правило, они разрушают стенку бактерии, которая ее защищает. И бактерия погибает.
- Не дают микроорганизмам расти и размножаться. Это так называемые бактериостатические антибиотики.
Они действуют на оболочку, через которую микроорганизм получает питание и выводит продукты обмена, – цитоплазматическую мембрану. В результате нарушается обмен веществ бактерии и она перестает развиваться. Еще одно действие бактериостатических антибиотиков направлено на подавление синтеза белка в бактерии. Результат тот же – клетка как бы замирает.
На что действуют и не действуют антибиотики
В основном инфекции вызываются бактериями, вирусами и грибами. Антибиотики действуют на разные виды бактерий и на грибы. Антибиотики не работают против вирусов.
Чтобы понять, почему антибиотики бессильны против вирусных инфекций, надо представлять себе, что такое бактерия и вирус.
Бактерия – одноклеточный микроорганизм, то есть клетка, обитающая в организме – на коже и слизистых. Болезнетворные бактерии могут проникать в плазму крови человека (бактериемия). Антибиотик проникает в бактерию-клетку и производит свое разрушительное действие.
Вирус намного меньше бактерии, его даже не увидишь в обычный микроскоп, только в электронный. Он представляет собой ДНК или РНК (нуклеиновые кислоты, несущие генетическую информацию), заключенную в оболочку из белка. Существовать вирус способен исключительно в чужой клетке. Проникая в нее и встраиваясь в ее геном, он начинает размножаться, вызывая болезнь.
Антибиотики назначают при бактериальных инфекциях различных органов и систем:
- дыхательной – бронхиты, пневмония;
- мочевыделительной – цистит, пиелонефрит;
- пищеварительной – язвенная болезнь, гастрит;
- нервной – энцефалит, менингит;
- лор-органов – ангины, отит, синусит;
- кожи – фурункулы.
Специальные антибиотики работают против грибковых инфекций, туберкулеза, сифилиса.
При заболеваниях, вызванных вирусами, антибиотики назначают, если к вирусной присоединяется бактериальная инфекция.
Когда антибиотики оказываются бессильны?
- Антибиотики не помогут в случае вирусных заболеваний: гриппа, ОРВИ, детских инфекций (корь, свинка, краснуха и пр.), ВИЧ и пр.
- Антибиотик может не подействовать, если он выбран неправильно. Так, есть антибиотики широкого и узкого спектра действия.
Первые работают против различных патогенных микроорганизмов, вторые действуют направленно только на определенные группы бактерий. Так, например, препараты пенициллина будут эффективны против грамположительных бактерий, но не помогут при туберкулезе или инфекции, вызванной грамотрицательными бактериями.
- Конкретный антибиотик может оказаться бесполезным, если патогенный микроорганизм обладает к нему резистентностью, то есть устойчивостью. Такая устойчивость возникает под действием мутаций бактерий в результате постоянного приема препарата. Бактерии – живые организмы, и им свойственно приспосабливаться к изменяющимся условиям.
Это свойство и вызывает резистентность к определенному антибиотику. Более того, бактерии могут передавать такую устойчивость своим следующим поколениям, и тогда препарат перестает работать против определенной бактериальной инфекции.
- Антибиотик не поможет, если принимать его неправильно.
Во-первых, такие препараты принимаются курсом – 3, 5, 7 дней, иногда больше. Нельзя самовольно сокращать курс, прекращать прием, если вы почувствовали себя лучше. Иначе болезнь возвратится, более того, к этому препарату разовьется резистентность.
Во-вторых, пить антибиотики нужно через строго определенные промежутки времени.
Если прием назначен один раз в день, то в один и тот же час; если два раза – через 12 часов, если три раза – через 8. Требование это вызвано тем, что антибиотик в организме работает конкретный период времени и когда действие одной таблетки заканчивается, надо принять следующую, чтобы процесс не прерывался.
Антибиотики – мощное средство против многих тяжелых инфекций. Но чтобы они работали, принимать их надо, если пропишет врач, и придерживаясь четкой схемы. Иначе они не только не помогут, но и нанесут вред.
