Вакуолизация в цитопл. Моноцитов
Что означает токсическая зернистость нейтрофилов в крови?
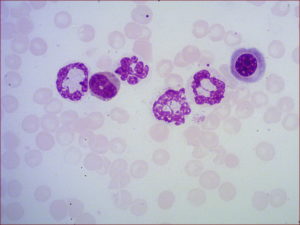
Самая большая разновидность популяции лейкоцитных клеток – нейтрофилы, по своему морфологическому строению относятся к группе гранулоцитов. Зрелые нейтрофильные клетки содержат многочисленные и разнообразные гранулы, всего около 300 видов, получившие название нейтрофильной зернистости.
Зернистость нейтрофилов участвует в выполнении двух основных функций этих клеток:
- в фагоцитном биохимическом расщеплении бактерий, грибов, вирусов и других микроорганизмов;
- в нетозном захвате и уничтожении ДНК-ловушками патогенных агентов некоторых аутоиммунных заболеваний.
Ввиду этого, изменение в структуре зернистости может быть признаком патологического процесса, и свидетельствовать о его тяжести.
Токсигенная зернистость является дегенеративной формой изменения морфологической структуры и свойств нейтрофилов, и считается клиническим признаком воздействия некоторых инфекционных агентов на внутриклеточные цитоплазматические белки.
Токсическая зернистость нейтрофилов состоит из специфических включений: пыли, хлопьев и/или очень крупных грубых гранул, которые содержат незрелые мукополисахариды, с размерами и формой, как у азурофильных нейтрофильных зёрен. Все такие включения окрашены в синевато-сиреневый цвет, наподобие базофильного оттенка. В норме же, нейтрофилы содержат небольшое количество нежных мелких зёрен бледно-розового тона.
Причины появления
К основным причинам возникновения токсической нейтрофильной зернистости относят:
- бактериальные, тяжёлые вирусные инфекции и воспалительные процессы;
- иммунодефицитные состояния;
- тяжелые гнойно-септические процессы и все септические заболевания;
- болезни приводящие к нарушению кроветворения;
- воздействие отравляющих веществ и химических препаратов;
- воздействие радиоактивного облучения, в том числе и лечебное.
Дегенеративная зернистость нейтрофилов особо выражена во время скарлатины, крупозного воспаления лёгких, гнойно-септических заболеваниях: при перитоните, флегмоне, септикопиемии, а также в процессе рассасывания инфильтратов и распаде злокачественных опухолей.
Важно! Морфологические изменения в цитоплазме и возникновение токсогенной зернистости не всегда обусловлены токсическим воздействием микроорганизмов. Они могут быть вызваны усиленной выработкой нейтрофилов и временем сокращения их созревания, которые не вызваны патогенами.
Следует также отметить, что к появлению токсической зернистости в нейтрофилах могут привести инфекционные и воспалительные заболевания, которые вызывают падение уровня нейтрофилов в крови, и требуют лечения колониестимулирующими препаратами.
Диагностика
Для точного установления наличия даже мелкой токсогенной пыли, а также для облегчения подсчёта количества нейтрофильных лейкоцитов с дегенеративной зернистостью, применяют специальные методики окрашивания.
В большинстве лабораторий используют технику по методу Е. Фрейфельд — подсчёт проводят по специальному запросу врача, во время составления лейкоцитарной формулы, при выполнении развёрнутого общего анализа крови.
Результат измеряется в % – подсчитывается количество клеток со специфическими вкраплениями на 100 нейтрофильных клеток. В лейкограмме указывается и оценка токсической зернистости в нейтрофилах – легкая, средняя и выраженная.
В бланке анализа обязательно описывается тип и размеры дегенеративных вкраплений, по которым также судят о тяжести течения заболевания:
- грануловидный, пылевидный или хлопьевидный;
- мелкие, средние или крупные.
Прогностическая значимость
Токсическая зернистость нейтрофилов – это ответная реакция организма на патологический процесс, а определение её наличия является важным потому, что такое дегенеративное изменение в клетках достаточно часто появляется раньше, чем лейкоцитный ядерный сдвиг.
В большинстве случаев, токсогенная зернистость – это:
- Предшественница нейтрофилии – повышения абсолютного или относительного количественного содержания нейтрофилов;
- Сдвига лейкоцитарной формулы влево;
- Появления в крови большого количества незрелых или палочкоядерных нейтрофилов, а также юных клеточных форм — метамиелоцитов и миелоцитов.
Кроме этого, нарастание % уровня деградации нейтрофильной зернистости говорит о развитии бактериемии и генерализации инфекции.
Если количество нейтрофилов с такой токсогенной зернистостью при гнойно-септических заболеваниях, крупозной пневмонии и некоторых других воспалительных болезнях превышает 50%, а при повторном анализе их процент ещё и повышается, то это свидетельствует о тяжёлом протекании инфекционной патологии и является плохим прогностическим клиническим симптомом.
Токсогенная зернистость нейтрофилов выступает важным клиническим симптомом во время диагностики следующих заболеваний:
- синдроме острого живота, в частности – гангренозный аппендицит;
- у ребёнка – болезнь Чедиака-Хигаси.
Оценивая динамику токсической зернистости, врач также судит об эффективности назначенного лечения, и, в случае необходимости, принимает решение о коррекции выбранной схемы медикаментозной терапии.
Другие виды токсогенных изменений
Помимо собственно токсогенной зернистости, усиленная стимуляция развития нейтрофильных клеток и сокращение времени на их развитие в красном костном мозге приводит и к другим проявлениям деградациям цитоплазмы.
Базофилия цитоплазмы
Такое морфологическое изменение цитоплазмы считается предтечей возникновения всех токсогенных разновидностей и выглядит как нерегулярные диффузные синие полоски. Вызывается присутствием полирибосом и эндоплазматического ретикулума.
Тельца Князькова-Деле или органы Деле
Представляют собой крупные, бледно-голубые, шероховатые участки в цитоплазме, которые свободны от гранул и пузырьков. Эти «глыбки» являются остатками эндоплазматической РНК-сети.
Чаще всего образуются во время скарлатины, кори, при сепсисе и обширных ожогах или обморожениях. Как правило, возникают вместе с токсогенной зернистостью и/или вакуолями.
В большинстве случаев, появление телец Деле – это самый ранний признак токсических нейтрофильных изменений.
Вакуолизация цитоплазмы
Образование вакуолей – пустот с нечёткими краями, встречается реже чем дегенеративная зернистость. Присутствие вакуолей строго коррелирует с наличием бактерий, которые нарушают функциональную работу нейтрофилов. Вакуолизация цитоплазмы возникает из-за дегрануляции лизосом и придаёт ей вид, похожий на пену.
Наличие вакуолей имеет важное диагностическое значение для определения сепсиса вызванного анаэробными инфекциями, абсцессов и острых дистрофических процессов в печени.
Синдром Чедиака-Хигаси
Наличие в цитоплазме нейтрофилов большого количества гранул с гигантскими размерами и причудливыми формами, а также ослабленная пигментация глазной радужки, кожных покровов и повышенная склонность к кровотечениям, указывает на наследственную болезнь Чедиака-Хигаси.
Дегенеративные изменения нейтрофилов
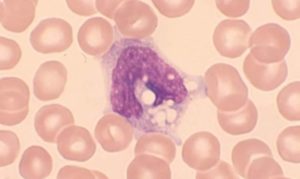
Дегенеративные изменения нейтрофилов возникают при различных патологических состояниях (инфекциях, воздействии химических веществ, заболеваниях кроветворного аппарата, действии проникающих излучений, попадании внутрь радиоактивных веществ и др.) и могут затрагивать и ядро, и цитоплазму. К ним относятся:
Токсическая (токсогенная) зернистость нейтрофилов — грубая зернистость, сходная с азурофильными гранулами.
Образование ее происходит внутри клетки в результате физико-химических изменений белковой структуры цитоплазмы под влиянием продуктов интоксикации. Наблюдается при инфекционных или воспалительных процессах.
Может сопровождаться присутствием цитоплазматических вакуолей и телец Деле.
Токсическая зернистость нейтрофилов нередко появляется раньше ядерного сдвига.
Ее нарастание при гнойно-септических заболеваниях, крупозной пневмонии и ряде воспалительных заболеваний указывает на прогрессирование патологического процесса и возможность неблагоприятного исхода.
В большом количестве токсическая зернистость нейтрофилов появляется при распаде опухолевой ткани под влиянием лучевой терапии.
Наиболее выражена токсическая зернистость при крупозной пневмонии в период рассасывания воспалительного инфильтрата, при скарлатине, септикопиемии, перитоните, флегмоне и прочих гнойных процессах. Особенно важное значение имеет она в диагностике острого живота (например, гангренозного аппендицита, протекающего с незначительно повышенной температурой тела и, нередко, при отсутствии лейкоцитоза).
Токсическую зернистость нейтрофилов можно обнаружить при окраске мазков обычным способом.Однако, даже при качественной окраске, пылевидная токсогенная зернистость может быть не видна, а при перекрашивании мазка (даже незначительном) за токсогенную можно принять специфическую зернистость нейтрофильных гранулоцитов.
Поэтому для выявления токсической зернистости нейтрофилов предложены специальные методы окраски, из которых наиболее распространенным и доступным является метод Фрейфельд
Метод Фрейфельд
Для окраски мазка используют следующие красители:
- 1 г основного фуксина растворяют при слабом нагревании в 15 г этилового спирта (96), охлаждают и добавляют 100 мл 5% раствора карболовой кислоты.
- 1% водный раствор метиленового синего.
Рабочую смесь готовят непосредственно перед окраской, так как она непригодна для хранения. К 20 мл водопроводной воды приливают 7 капель первой краски, смешивают, прибавляют 5 капель второй краски и снова перемешивают.
Мазки крови, фиксированные в течение 3 минут метиловым спиртом, красят в течение 1 часа приготовленной рабочей смесью красителя, а затем смывают водой и высушивают. Препарат, уже окрашенный по Романовскому, может быть окрашен этим способом без предварительного обесцвечивания.
В результате такой окраски в цитоплазме нейтрофилов выявляется синеватая зернистость различного размера (от пылевидной до хлопьевидной) в зависимости от тяжести патологического процесса.
Подсчитывают количество клеток с токсической зернистостью в процентах (на 100 нейтрофильных гранулоцитов).
В анализе указывают также величину зернистости (пылевидная, мелкая, средняя, крупная, хлопьевидная).
Токсическая зернистость нейтрофилов (фотографии)
Toxic monocyte, toxic neutrophils, sepsis
Тельца (включения) Деле (Князькова-Деле, Доули) — светло-синие глыбки различного размера и формы, представляющие собой РНК из фрагментов шероховатого эндоплазматического ретикулума. Появляются при инфекционных и воспалительных заболеваниях (иногда даже при легком течении). Часто встречаются в сочетании с токсической зернистостью и цитоплазматическими вакуолями.
Тельца Деле (микрофотографии)
Dohle bodies
Dohle bodies
Цитоплазматические вакуоли — наблюдаются при тяжелых инфекциях, часто в сочетании с токсической зернистостью и тельцами Деле. При остром сепсисе, вызванном анаэробной инфекцией, и выраженном лейкоцитозе наблюдается вакуолизация практически всех нейтрофилов. Иногда вакуолизация выявляется при аномалии Джордана (семейной вакуолизации лейкоцитов).
Вакуолизация (микрофотографии)
Abnormal late neutrophils, colorless cytoplasm, M-7 leukemia
Cytoplasm is vacuolated
Гиперсегментация сегментоядерных нейтрофилов — ядро имеет более пяти долей, соединенных тонкой хроматиновой нитью. Встречаются при мегалобластных анемиях. Может отмечаться (редко) у здоровых людей как наследственная (семейная) конституциональная особенность.
Гиперсегментация нейтрофилов (фотографии)
Hypersegmented and normal segmented neutrophil
Hypersegmented neutrophil buffy coat of pernicious anemia
Hypersegmented neutrophil leukocytosis
Гипосегментация ядра (пельгероид, псевдопельгеровская аномалия) — увеличение количества двусегментированных нейтрофилов, а также палочкоядерных нейтрофилов и нейтрофилов с круглым ядром. При этом хроматин имеет плотную структуру.
Встречается при лейкозах, миелопролиферативных заболеваниях, МДС, агранулоцитозе, множественной миеломе, микседеме, малярии, при инфекционных заболеваниях, при приеме некоторых лекарственных препаратов. Образование их связывают с блокадой ферментов, ответственных за сегментацию ядер.
Следует отличать от пельгеровской аномалии (при пельгероиде изменения со стороны нейтрофилов носят непостоянный характер, в отличие от пельгеровской аномалии).
Пельгероид, псевдопельгеровская аномалия (фотографии)
Blasts Pelgeroid neutrophils AML in relapse
Pelgeroid neutrophils blasts AML in relapse
Кольцеобразные ядра — ядра имеют форму кольца. Наблюдаются при тяжелом алкоголизме.
Хроматинолиз — при распаде хроматин теряет свою нормальную структуру — растворяется. Ядро окрашивается в светлый цвет, контуры его сохраняются.
Кариолиз — растворение лишь части ядра с сохранением его нормальной структуры. В местах растворения ядро теряет способность окрашиваться основными красками, контуры его нечеткие, размытые.
Фрагментоз — процесс при котором от ядра отделяются отдельные фрагменты (частицы). Они могут быть связаны с ядром тонкими нитями базихроматина.
Пикноз — уплотнение базихроматина ядра. Ядро при этом становится темным, бесструктурным. Размер клетки уменьшается. Процесс пикнотизации распространяется либо на все ядро, либо на отдельные его участки или сегменты.
Кариорексис — распад ядра на отдельные части, не связанные между собой, округлой формы и резко пикнотичные, темные бесструктурные образования.
Кариорексис (микрофотографии)
Band neutrophils karryorexes of neutrophils smudge cells
Цитолиз — распад клетки. Цитоплазма чаще отсутствует. Ядро теряет свою обычную структуру, контуры его расплывчатые. В тяжелых случаях можно обнаружить только остатки ядра и зернистость.
- Л. В. Козловская, А. Ю. Николаев. Учебное пособие по клиническим лабораторным методам исследования. Москва, Медицина, 1985 г.
- Фред Дж. Шиффман. «Патофизиология крови». Пер. с англ. — М. — СПб.: «Издательство БИНОМ» — «Невский Диалект», 2000 г.
- Руководство к практическим занятиям по клинической лабораторной диагностике. Под ред. проф. М. А. Базарновой, проф. В. Т. Морозовой. Киев, «Вища школа», 1988 г.
- Руководство по клинической лабораторной диагностике. (Части 1 — 2) Под ред. проф. М. А. Базарновой, академика АМН СССР А. И. Воробьева. Киев, «Вища школа», 1991 г.
- Справочник по клиническим лабораторным методам исследования. Под ред. Е. А. Кост. Москва «Медицина» 1975 г.
К морфологически идентифицируемым клеткам эритроцитарного ростка относятся эритробласт, пронормоцит, нормобласты (базофильные, полихроматофильные и оксифильные), ретикулоциты и эритроциты.
Раздел: Гемоцитология
Читать
Монобласт — родоначальная клетка моноцитарного ряда. Размер 12 — 20 мкм. Ядро большое, чаще круглое, нежносетчатое, светло-фиолетового цвета, содержит 2 — 3 ядрышка. Цитоплазма монобласта сравнительно небольшая, без зернистости, окрашена в голубоватые тона.
Раздел: Гемоцитология
Читать
Пельгеровская аномалия нейтрофилов — изменение крови, наследуемое по доминантному типу. Особенность развития пельгеровских лейкоцитов выражается главным образом в морфологическом изменении ядер нейтрофилов — нарушении процесса их сегментации (ядро старое, а форма его юная).
Структура ядер пельгеровских нейтрофилов грубоглыбчатая, пикнотическая. Большинство пельгеровских нейтрофилов имеет однодолевое, несегментированное ядро, по форме сходное с палочкоядерными клетками, а также в виде эллипса, окружности, боба или почки, оно короче, чем у обычного нейтрофила.Реже встречаются ядра с намечающейся перетяжкой посередине, напоминающие по форме гимнастическую гирю или земляной орех.
Раздел: Гемоцитология
Читать
Тельца Жолли (тельца Хауэлла-Жолли) — мелкие круглые фиолетово-красные включения размером 1 — 2 мкм, встречаются по 1 (реже по 2 — 3) в одном эритроците. Предсталяют собой остаток ядра после удаления его РЭС. Выявляются при интенсивном гемолизе и «прегрузке» РЭС, после спленэктомии, при мегалобластной анемии..
Раздел: Гемоцитология
Читать
Основным местом образования лимфоцитов служит кроветворная ткань селезенки и лимфатических узлов. В костном мозге и периферической крови в норме встречаются только зрелые лимфоциты. При патологии в костном мозге и периферической крови могут появляться незрелые и атипические формы клеток лимфоидного ростка.
Раздел: Гемоцитология
Читать
Вакуолизация моноцитов
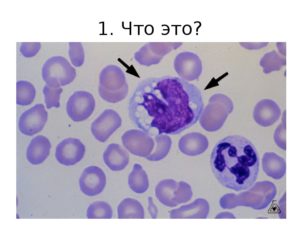
- Моноцит – крупнейшая клетка в циркулирующей крови (размером около 12-22 микрометров), она содержит большой объем цитоплазмы, которая окрашена в темно-серый цвет (часто называют “небо в день пасмурный”). Цитоплазма отличается мелкой азурофильной зернистостью, которая различима только при достаточной покраске мазка клетки.
- Ядро достаточно большое, обладает рыхлостью, полиморфностью, в виде трилистника, фасоли, подковы, встречается в виде такого насекомого, как бабочка с раскрытыми крыльями.
- Предшественница этих клеток (КОЕ-ГМ) единая с гранулоцитами, а сама предшественница именно моноцитарного ростка это КОЕ – М. Эти клетки покидают костный мозг, так полностью не созрев, живут в кровяном русле около 20-40 часов, потом они покидают периферическую циркулирующую кровь и перемещаются в ткани, там они полностью специализируются.
- Покинув кровоток, клетки не смогут снова вернуться обратно. Вышедшие в ткани моноциты становятся макрофагами (в некоторых органах имеют специфические названия, а именно: купферовские клетки печени, гистиоциты, содержащиеся в соединительной ткани, альвеолярные, плевральные макрофаги, остеокласты, микроглии нервной системы). В самих живых клетках органов они имеют возможность жить от месяца до многих лет.
- Движение моноцитов похоже на амебовидное, также они обладают фагоцитарной способностью. Переваривают не только собственные мертвые клетки, множество микроорганизмов и грибов, но и клетки, стареющие, такие как элементы крови, и зараженные вирусами.
- Они уничтожают за счет своих функций и строения очаг местного воспаления и создают условия для процесса репарации. Но в самом кровяном русле клетки почти не обладают своей фагоцитарной активностью.
- Помимо процесса фагоцитоза, моноциты обладают секреторной и синтетической способностями. Они способны синтезировать и вырабатывать совокупность таких факторов, как «медиаторы» воспаления: интерферон-a, интерлейкины-1,-6, ФНО-α.
Здесь вы найдете интересную информацию про метамиелоциты в крови.
Определение уровня моноцитов в крови
Общий анализ крови (ОАК) в настоящее время является самым популярным скрининговым анализом, который требовалось сдавать, наверное, любому человеку.
Он постоянно применяется в качестве скринингового, одного из важнейших первичных методов исследования при самой разнообразной величине патологических состояний, поэтому для определения уровня этих клеток используется именно он.
Этот анализ позволяет определить общее число всех лейкоцитов и пропорциональное соотношение различных форм среди них, это называется определением лейкоцитарной формулы.
Специфической подготовки к обследованию нет. Желательно сдавать анализ утром натощак или через два часа после приема пищи.
Норма моноцитов в крови
Они представляют собой особую категорию лейкоцитов и определяются как относительным (в процентном соотношении к общему числу лейкоцитов), так и в абсолютном количестве.
Общий анализ крови позволяет посчитать относительное число, но существуют специальные методы, которые позволяют определить абсолютное число клеток на единицу объема (чаще литр крови). Причем число клеток не имеет половой зависимости, иногда даже и возрастной.
Соотношение моноцитов в крови человека представлено в таблице ниже:
| Возраст | До 1 года | До 12-ти лет | После 12-ти лет и у взрослых |
| Относительное количество | 2-12 % | 3-9 % | 3-11 % |
| Абсолютное количество | 0,12-1,8 *109/л | 0,15-1,08 *109/л | 0,12-0,99 *109/л |
Узнайте, как поднять лейкоциты, прочитав нашу аналогичную статью.
Снижение количества моноцитов
О снижении этих клеток (такой симптом называется моноцитопенией) можно говорить, когда число этих клеток падает до 1% и ниже. В настоящее время такие состояния встречаются нечасто.
Наиболее частые основания для изменений этих клеток, это:
- период вынашивания плода и роды (если говорить о беременности, то стоит указать, что в 1-м триместре у всех женщин выявляется значительное уменьшение всех форменных клеток крови и в том числе и моноцитов, а в момент родов происходит истощение всех резервных ресурсов в организме);
- ослабление организма (при различных диетах, хронических заболеваниях; пристально нужно следить за снижением моноцитов в детском возрасте, потому что будет нарушена жизнедеятельность всех внутренних систем и органов, и детский организм в последующем будет не полностью развиваться);
- действие химиотерапевтических препаратов и состояния после лучевого воздействия (развивается апластическая анемия, чаще бывает у женщин);
- осложненные гнойные состояния и острые инфекционные процессы (к примеру, сальмонеллез).
Что значат повышенные моноциты?
Если их больше нормы, выше 11% (такой симптом называется моноцитозом), то это говорит о присутствующих инородных микроорганизмах или агентах, что является специфическим для инфекционных состояний и различных по гистологической природе опухолей.
Источниками моноцитоза могут быть следующие состояния:
- инфекционный мононуклеоз;
- острые воспалительные заболевания инфекционной природы (дифтерия, грипп, краснуха, корь) на ранних этапах реконвалесценции – инфекционный моноцитоз;
- специфические заболевания (сифилис, туберкулез);
- лимфомы;
- системные расстройства развития соединительной ткани (красная волчанка);
- лейкозы.
- протозоонозы и риккетсиозы (лейшманиоз, малярия);
- послеоперационный период (особенно после обширных операций на органах желудочно-кишечного тракта, органах грудной полости).
Инфекционный мононуклеоз (ИМ) — острое вирусное расстройство, которое вызывается вирусом Эпштейн-Барра (является герпес вирусом 4 типа).
Инкубационный период длится от 2-х недель до 2-х месяцев.
Главный симптомокомплекс содержит данные особенности:
- увеличение размеров периферических лимфоидных участков, в особенности шейной группы;
- патологические процессы в носоглотке и ротоглотке;
- лихорадку;
- возникновение мононуклеаров в периферической крови;
- увеличение объемов печени и селезенки.
Помимо главных симптомов при ИМ могут присутствовать такие: энантема, экзантема, пастозность век, одутловатость лица, ринит. Расстройство начинается остро, с возникновения лихорадки. Обычно все симптомы развиваются к концу 6-7 дня.
Самыми начальными клиническими проявлениями являются:
- поднятие температуры тела;
- налет на небных миндалинах;
- воспаление и увеличение шейных лимфатических узлов;
- затруднение дыхания.
К концу 7-8 дня от момента развития недуга у большинства людей уже можно пропальпировать увеличенную и уплотненную печень и селезенку, в клиническом анализе крови уже начинают появляться атипичные мононуклеары. В некоторых отдельных случаях болезнь развивается постепенно.
Осложнения:
- Специфические: удушье, серозный менингит, разрыв селезенки, поражение нервной системы, тробоцитопения, агранулоцитоз, гемофагоцитарный синдром, инфекционно-токсический шок.
- Бактериальные: отит, мастоидит, паратонзиллит, гнойный лимфаденит.
Возможно несколько исходов острого инфекционного процесса:
- реконвалесценция
- бессимптомное вирусоносительство либо скрытая инфекция
- затяжная рецидивирующая инфекция:
Лабораторная диагностика:
- Изменения периферической крови: лейкоцитоз, умеренное повышение СОЭ, лимфомоноцитоз.Самым главным и специфическим признаком инфекционного мононуклеоза являются атипичные мононуклеары, доля которых становится выше 20%. Они появляются к 10-14 дню болезни и сохраняются до 1 месяца.
В аналогичной статье мы отвечаем на вопрос, что делать, если повышен СОЭ у женщин.
Лечение симптоматическое. В начальном моменте следует рекомендовать постельный режим, на этапе реконвалесценции — сдерживание физической нагрузки. С противовоспалительной целью назначают НПВС в рекомендуемой дозировке. В острую стадию процесса не показано назначение противовирусных препаратов (препараты ацикловира).
Назначение ГКС показано при развитии осложнений (обструкция в.д.п., тромбоцитопении, гемолитической анемии, поражении ЦНС). Назначение АБ показано при присоединении вторичной бактериальной флоры. Сторониться назначения аминопенициллинов. Следует гарантировать присмотр за полостью рта.
Симптомы и виды моноцитоза
Такое состояние – моноцитоз, можно разделить на несколько видов:
- Абсолютный моноцитоз: его возможно диагностировать, когда количество самих клеток становится выше 0,12-0,99*109/л.
- Относительный моноцитоз: состояние патологическое или физиологическое, при котором общая часть моноцитов становится выше 3-11% от общего числа лейкоцитов.
Причем абсолютные цифры содержания моноцитов могут оставаться в границах нормы, но будет повышен их уровень в общей лейкоцитарной формуле, это значит, что количество моноцитов будет прежним, но будет снижена численность других видов лейкоцитов. Чаще такое наблюдается при снижении числа нейтрофилом (нейтропении) и снижении числа лимфоцитов (лимфоцитопении).
Абсолютный моноцитоз представляет собой важность при выявлении и терапии патологических процессов в сравнении с относительным, который может меняться в зависимости от травм, стрессов, питания.
Моноцитоз при беременности: у женщин, вынашивающих плод, не слишком высокое увеличение суммы лейкоцитов и моноцитов считается физиологической реакцией организма на “чужеродное” тело. И нужно всегда иметь ввиду, что абсолютный моноцитоз у беременных следует обязательно корректировать в отличие от относительного.
Моноцитоз – не заболевание, а симптом основной болезни. Поэтому картина моноцитоза будет зависеть от самого заболевания.
В отсутствие любых симптомов болезни его можно распознать по неспецифическим признакам:
- хроническая усталость,
- быстрая утомляемость
- сниженная работоспособность,
- общая слабость,
- сонливость,
- постоянная субфебрильная температура.
Эти признаки могут указывать на разнообразные заболевания. При беременности они являются физиологически обусловленными.
В любом случае требуется обратиться к врачу и сдать анализы.
В чем опасность заболевания?
Если в проведенном анализе содержание этих клеток увеличено, то это указывает на изменения в иммунной системе, а именно начало иммуносупрессии. Поэтому требуется необходимая профилактика, а зачастую и терапия данных расстройств.
Инфекционные болезни без этиотропной и патогенетической терапии могут привести к тяжелым последствиям, развитию осложнений, отягощению существующих состояний и самих заболеваний.
Несвоевременное диагностирование онкологических процессов также приводит к развитию тяжелых последствий, инвалидизации, летальности. Поэтому целесообразно обратиться к специалистам с консультацией и решением вопроса о своевременной диагностике, постановке диагноза и терапии.
Одновременное повышение других лейкоцитов на фоне моноцитоза
- Повышение нейтрофилов в особенности палочкоядерных (нейтрофилез). Такого рода процесс показывает на острое воспалительное расстройство и наиболее выражено при гнойных процессах (менингите, абсцессах и флегмонах, рожистом воспалении).
- Повышение лимфоцитов (лимфоцитоз), состояние, которое характерно для отдельного ряда инфекций. Если лимфоциты повышены у взрослого, о чем это говорит?
- Повышение эозинофилов (эозинофилия) указывает на присутствие аллергических заболеваний и синдромов, паразитарных заболеваний, кожных болезней, коллагенозов, многих тяжелых заболеваний крови, специфических воспалительных заболеваний.
Что делать при возникновении патологии?
Повышение уровня моноцитов является в любом случае обязательным поводом прибегнуть к помощи специалиста – врача для дальнейшего выяснения причин такого состояния. Даже несильное повышение уровня фагоцитов должно вызвать настороженность.
В первую очередь понадобится еще раз пересдать общий анализ крови с целью выявления повышения остальных показателей или только узкое повышение моноцитов. И при выявлении повторного повышения их обязательно дообследоваться и выяснить первопричину моноцитоза.
Лейкоциты — Дегенеративные изменения лейкоцитов — Клетки крови — виды, строение, функции
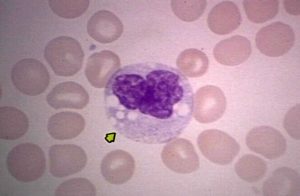
Характеризуются отложением в клетках различных эндо- и экзогенных веществ, в результате чего они теряют способность к нормальному функционированию и делению. Патологические вещества, депонирующиеся в клетке и вызывающие дегенеративные изменения лейкоцитов, могут быть различными по своей природе:
- липиды (жировая дегенерация);
- пигменты (пигментная дегенерация) и пр.
Важное значение в клинической практике имеет исследование как морфологического состава лейкоцитов, так и их функционального состояния, наличия дегенеративных изменений.
К дегенеративным изменениям лейкоцитов относятся токсогенная зернистость нейтрофильных гранулоцитов (ТЗН), вакуолизация, появление телец Князькова—Деле, зерен Амато и др.
Токсогенная зернистость нейтрофильных гранулоцитов
Формирование специфической зернистости нейтрофильных гранулоцитов начинается в комплексе Гольджи. Размеры гранул колеблются от 0,2 до 0,5 мкм, форма их округлая или слегка продолговатая.
Округлую, первичную, зернистость содержат незрелые клетки нейтрофильного ряда — промиелоциты; продолговатую, вторичную, специфическую — зрелые нейтрофильные гранулоциты — палочкоядерные и сегменто-ядерные.
В миелоцитах и метамиелоцитах обнаруживаются как первичные, так и вторичные гранулы.
Образование токсогенной зернистости происходит внутри клетки в результате физико-химических изменений белковой структуры цитоплазмы под влиянием продуктов интоксикации.
Появление ее объясняется выходом в периферическую кровь незрелых нейтрофильных гранулоцитов костного мозга, содержащих первичные гранулы, богатые белками, обладающими бактерицидными свойствами, а также гликозамингликанами и лизином.
Токсогенная зернистость нейтрофильных гранулоцитов нередко появляется раньше ядерного сдвига. Ее нарастание при гнойно-септических заболеваниях, крупозной пневмонии и ряде воспалительных заболеваний указывает на прогрессирование патологического процесса и возможность неблагоприятного исхода.
В большом количестве токсогенная зернистость нейтрофильных гранулоцитов появляется при распаде опухолевой ткани под влиянием лучевой терапии. Наиболее выражена токсогенная зернистость при крупозной пневмонии в период рассасывания воспалительного инфильтрата, при скарлатине, септикопиемии, перитоните, флегмоне и прочих гнойных процессах.
Особенно важное значение имеет токсогенная зернистость в диагностике острого живота (например, гангренозного аппендицита, протекающего с незначительно повышенной температурой тела и нередко при отсутствии лейкоцитоза). При описании токсогенной зернистости (мазок крови окрашивается карболфуксинметиленовым синим по Е. О.
Фрейфельд) указывают процент содержащих ее клеток и размеры зернистости (мелкая, среднего размера, крупная, хлопьевидная).
Тельца Князькова—Деле
Тельца Князькова—Деле обнаруживаются в цитоплазме нейтрофильных гранулоцитов в виде довольно крупных бледно-голубых комочков различной формы. Встречаются они при воспалительных и инфекционных заболеваниях, протекающих даже в легкой форме, когда токсогенная зернистость еще слабо выражена или совсем отсутствует.
Существует несколько точек зрения по поводу происхождения телец Князькова—Деле. Согласно одной из них, они имеют ядерное происхождение, другой — являются остатками базофильной спонгиоплазмы юных клеток, третьей —того же происхождения, что и токсогенная зернистость.
Зерна Амато
Зерна Амато выявляются в цитоплазме нейтрофильных гранулоцитов в виде небольших округлых, овальных или похожих на запятую образований, окрашивающихся в бледно-голубой цвет и содержащих красные или красно-фиолетовые зерна. Появляются они при скарлатине и других инфекционных заболеваниях. По происхождению их считают близкими к тельцам Князькова—Деле.
Аномалия лейкоцитов Пельгера
Впервые была описана голландским гематологом Пельгером в 1830 г. В настоящее время встречается довольно часто. Наследование этой аномалии осуществляется по доминантному типу от одного из родителей (гетерозиготы) или, что встречается редко, от обоих (гомозиготы).
В крови страдающих этой аномалией обнаруживается огромное количество круглоядерных лейкоцитов. Теоретически вероятность гомозиготного варианта пельгеровской аномалии составляет 1:1000000, фактически она встречается еще реже.
Описаны всего четыре случая достоверных гомозиготов. При гетерозиготном наследовании аномалия передается из поколения в поколение и определяется у 50 % членов семьи. Таким образом, наличие у отдельных членов семьи нормальной лейкограммы не противоречит семейно-наследственному характеру аномалии.
Особенностью лейкоцитов при аномалии Пельгера является форма ядра.
Большинство нейтрофильных гранулоцитов имеют однодолевое несегментированное эллипсовидное, бобовидное или почкообразное ядро, более короткое, чем ядро обычного нейтрофильного гранулоцита.
В других клетках ядра с намечающейся перетяжкой посредине напоминают по форме гимнастическую гирю или земляной орех (арахис).
Бывают также клетки с ядрами, переходными к двусегментарным (имеющим вид пенсне); ядра с тремя сегментами почти не встречаются.Как дву-, так и трисегментоядерные формы отличаются короткими перемычками и комковатым строением ядра. Нейтрофильные гранулоциты с большим количеством сегментов при аномалии Пельгера не встречаются.
Наряду с несегментированными, палочкоядерными и сегментоядерными нейтрофильными гранулоцитами наблюдаются и кругло-ядерные, которые признаны вполне зрелыми клетками. Особенность их развития заключается в полном отсутствии ядерного полиморфизма, т. е.
ядро их по структуре хроматина старое, а по форме — юное.
Во избежание ошибочной трактовки анализа при наличии указанных форм нейтрофильных гранулоцитов врач-лаборант обязан дать заключение о том, что описанная картина крови характерна для аномалии лейкоцитов Пельгера.
При наличии подобных изменений формы ядра в эозинофильных и базофильных гранулоцитах эти клетки также подсчитываются дифференцированно (круглоядерные, несегментированные, палочкоядерные, двусегментоядерные и трисегментоядерные).
По физиологическим свойствам лейкоциты при аномалии Пельгера ничем не отличаются от обычных. У женщин — носителей этой аномалии половой хроматин не выявляется.
У женщин — частичных носителей аномалии могут наблюдаться нейтрофильные гранулоциты с половым хроматином (последний в виде телец Барра обнаруживается и в ядрах клеток слизистой оболочки полости рта, в которых обычно исследуется половой хроматин).
Указанный феномен объясняется задержкой сегментации ядер пельгеровских нейтрофильных гранулоцитов, вследствие чего половой хроматин остается как бы замурованным в массе ядра.
В костном мозге преобладают круглоядерные нейтрофильные гранулоциты (до 65 %). Среди них обнаруживаются зрелые клетки с круглым, овальным или эллипсоидным ядром.
Таким же образом происходит развитие характерных для аномалии Пельгера круглоядерных эозинофильных гранулоцитов.Эритрокариоциты составляют не более 15—20 %, причем встречаются почти исключительно нормобласты с пикнотическим ядром при различной степени гемоглобинизации.
Наряду с аномалией лейкоцитов Пельгера, носящей семейно-наследственный характер, в последние годы появились описания приобретенных форм гипосегментации ядер нейтрофильных гранулоцитов — пельгероидов.
Псевдопельгеровские лейкоциты, в отличие от истинных, в крови обнаруживаются непостоянно. Появление их связано с основным заболеванием.
Следует также помнить о возможности наличия у носителей пельгеровской аномалии одновременно и аномалии лейкоцитов Штодмейстера.
В отличие от типично пельгеровских круглоядерных нейтрофильных гранулоцитов с грубоглыбчатой фрагментированной структурой ядер, имеющих четкие контуры, ядра при аномалии Штодмейстера характеризуются менее выраженной конденсацией хроматина, наличием бухтообразной выемки и своеобразной бахромчатости, состоящей из нежных хроматиновых нитей, как бы выступающих из основной массы ядра в цитоплазму. Эта аномалия также носит семейный характер и может обнаруживаться не только при пельгеровском варианте, но и самостоятельно.
