Stenotrophomonas maltophilia
Инфекции, связанные со Stenotrophomonas maltophilia у пациентов отделений реанимации и интенсивной терапии » Журнал
Зубарев А.С.
Городская клиническая больница №40, Екатеринбург, отделение реанимации №3
Резюме
В результате анализа литературных данных установлено. Частота случаев инфекции, связанной со S. maltophilia в ОРИТ заметно возросла. Выбор антибактериальных препаратов для ведения таких инфекций представляет большую проблему для микробиологической лаборатории и клиницистов.
Методы выявления чувствительности бактерии к антимикробным препаратам часто дают неточные результаты и требуют дальнейшего совершенствования. Наибольший опыт терапии связан с использованием тикарциллинаклавуланата и триметопримсульфометаксазола. Значение альтернативных препаратов для ведения инфекции S. maltophilia, особенно новых фторхинолонов требует дальнейшего изучения.
Необходима оценка клинической эффективности комбинации антимикробных препаратов, показавших синергизм in vitro в отношении бактерии.
За последние три десятилетия в связи с интенсивным развитием медицинских технологий и совершенствованием оказания помощи при многих острых критических состояниях и декомпенсации хронических заболеваний, в ОРИТ увеличилось количество ослабленных больных с тяжелым соматическим фоном и инфекционными осложнениями. В свою очередь, в этих условиях, в результате необходимости использования антибиотиков широкого спектра существенно выросла значимость в качестве возбудителей нозокомиальных инфекций слабовирулентных микроорганизмов, обладающих природной резистентностью ко многим антимикробным препаратам.
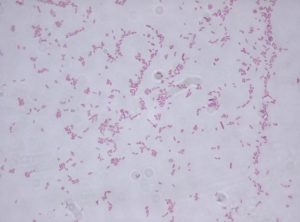
К таким микроорганизмам относится и Stenotrophomonas maltophilia, неферментирующая грамотрицательная бактерия, ранее известная как Pseudomonas maltophilia или Xanthomonas maltophilia.
Цель настоящего аналитического обзора — обобщение данных литературы, посвящённых значимости инфекций обусловленных Stenotrophomonas maltophilia у пациентов ОРИТ.
Микробиологическая характеристика
S. maltophilia — единственный представитель рода Stenotrophomonas (Stenos, греч. — узкий; trophos, греч. — питающаяся; monas, греч. — единица, организм; и malt, староанглийский — солод; philos, греч.- друг).
Название отражает ограниченную способность вида использовать питательные субстраты при способности образовывать кислые продукты из мальтозы («солодовый сахар»), что было использовано при разработке среды для селекции S. maltophilia.
Род был выделен в 1993 году Palleroni и Bradbury [58] после многолетних дебатов относительно таксономического положения этого микроорганизма.
Клетки S. maltophilia прямой или слегка изогнутой формы неспорообразующие грамотрицательные бациллы, от 0,5 до 1,5 мкм длиной. Они подвижны, благодаря наличию нескольких полярно расположенных жгутиков. Колонии гладкие, блестящие с ровными краями, белого или бледно-желтого цвета. S. maltophilia облигатный аэроб.
Рост не отмечается при температуре выше 40° С и ниже 5°. Оптимальная температура для роста — 35° С. Бактерия относится к относительно метаболически неактивным микроорганизмам (395), но может метаболизировать ряд необычных субстратов, включая аминогликозидный антибиотик стрептомицин [27].
Штаммы бактерии изучаются для потенциального использования в качестве биодеградантных агентов.
S. maltophilia широко распространена в окружающей среде и географических регионах, включая Антарктику [88], и занимает экологические ниши как внутри так и за пределами больниц.
Бактерия была выделена из большого количества нозокомиальных источников, включая контуры аппаратов искусственной вентиляции, руки персонала, аппараты диализа, небулайзеры, устройства для ингаляционной терапии и даже растворы дезинфектантов. Достаточно мало информации известно о способности S.
maltophilia переносить высушивание, однако Rosenthal сообщает, что хотя бактерия достаточно часто выделяется во влажной среде, обнаружение ее в сухих местах, таких как больничный пол, встречается нечасто [73].
S. maltophilia использовалась как агент биологического контроля среде с ризосферами и против агрокультурных паразитов. Учитывая ингибирование бактерией широкого спектра фитопатогенных грибов, не удивительно сообщение о том, что S.
maltophilia подавляет рост патогенных для человека грибов, таких как Candida spp. и Aspergillus fumigatus [39]. Jakobi с соавторами сообщали о выработке S.
maltophilia мальтофилина, нового макроциклического лактамного агента с антигрибковой активностью против сапрофитных, фитопатогенных и человеческих изолятов [35].
О факторах вирулентности S. maltophilia известно мало. Сложности с разделением колонизации и инфекции привело к формированию представления об ограниченной патогенности возбудителя.Описана выработка бактерией ряда внеклеточных ферментов, включая ДНКазу, РНКазу, фибринолизин, липазу, гиалуронидазу, протеазу и эластазу [8].
Сродство к пластику считается важным свойством бактерии, часто формирующей колонизацию и инфекцию вдоль инфузионных линий и внутривенных канюль [40]. Способность S.
maltophilia выживать и размножаться в растворах для парентерального питания и других типах инфузионных сред может также вносить вклад в патогенез ассоциированных с внутривенной линией инфекций. [52, 62]. Также известна способность бактерии к росту в диализных растворах с высвобождением низкомолекулярных пирогенов.
Эпидемиология
До недавнего времени, S. maltophilia считалась достаточно необычным микроорганизмом при выделении в диагностической микробиологической лаборатории. Частота выделения возросла с начала 1970-х годов. Вероятно, такой рост связан с достижениями медицинских технологий в результате чего увеличилось количество пациентов с имеющимися факторами риска развития инфекции (таблица 1) [54].
Таблица 1
Факторы риска инфекции, связанной со S. maltophilia [93]
В масштабном исследовании по изучению факторов риска развития нозокомиальных инфекций в ОРИТ, проводившемся в нескольких центрах в Германии наиболее значимыми выявленными независимыми факторами риска для выделения микроорганизма были предшествующее использование карбапенемов и длительное пребывание в ОРИТ (более 12 дней) [115]. В другом масштабном проспективном исследовании по методу случай-контроль, проведенном во Франции в период с 1998 по 2001 наиболее значимыми факторами риска были наличие хронических легочных заболеваний у пациента и предшествующая антибактериальная терапия. Уровень смертности в ОРИТ, продолжительность искусственной вентиляции и продолжительность пребывания в ОРИТ были значительно выше у пациентов с инфекцией S. maltophilia, по сравнению с группой контроля. В случае инфекции S. maltophilia смертность была значительно выше у пациентов, которым была назначена неадекватная антибактериальная терапия [94].
Особо сложной задачей для клиницистов является ведение ослабленных пациентов с инфекцией, вызванной полирезистентными микроорганизмами. Ansari с соав. изучили онкологических больных с инфекцией, вызванной полирезистентной S.
maltophilia и сравнили их двумя группами контроля: пациентами с факторами риска развития инфекции S. maltophilia (С-контроль), а также пациентами с инфекцией, вызванной S. maltophilia, чувствительной по меньшей мере к двум антибиотикам (S-контроль).
По сравнению с пациентами группы C-контроля, у больных с инфекцией, вызванной полирезистентной S. maltophilia значимо чаще использовались до выделения микроорганизма карбапенемы и фторхинолоны, они имели более длительное время пребывания в ОРИТ, и уровень смертности среди них был также значимо выше.
По сравнению с пациентами S-контроля, факторами риска были — предшествующие в течение года инфекция S. maltophilia и использование триметоприм-сульфаметоксазола [121].
Сравнение факторов риска между разными исследованиями затруднено из-за разнородности популяции пациентов, критериев, используемых для выявления инфекции и статистических методов, использованных для обработки данных.
Примечательно, однако, что некоторые из них, такие как предшествующее назначение антибактериальных препаратов, связываются с инфекцией S. maltophilia большинством авторов и что почти все факторы риска свидетельствуют о выраженном снижении антиинфекционной защиты пациента.Описано несколько серьезных вспышек инфекции и/или колонизации S. maltophilia. В нескольких случаях был выявлен источник загрязнения. Контаминированная дистиллированная вода, которая использовалась для изготовления дезинфицирующих растворов была установлена в качестве источника одной вспышки инфекции S.
maltophilia, в которую были вовлечены 63 пациента в одном австралийском госпитале [92]. Четыре случая септицемии S. maltophilia были связаны с недостаточной дезинфекцией многоразовых диализаторов [84].
У восьми пациентов гематологического отделения (четверо с лейкемией и четверо с множественной миеломой) с развившейся инфекцией S. maltophilia, таким источником стала морозильная камера [69]. Лед использовался для создания прохладных напитков и содержал высокую концентрацию бактерий (> 105 КФЕ/мл).
Клинические проявления инфекций
Спектр клинических проявлений, связанных с инфекцией S. maltophilia постоянно расширяется. Многие ранние публикации не могли установить четкие признаки инфекции, связанной с этим микроорганизмом.
Действительно, частое выделение бактерий в смешанных культурах, трудность разделения инфекции и колонизации в области поверхностных зон, таких как кожа или верхние отделы дыхательных путей сформировали мнение, встречающееся в ранних публикациях, о том, что S. maltophilia является организмом со строго ограниченным патогенным потенциалом.
Однако, более поздние исследования, в которых использовались строгие критерии определения инфекции, связанной с выделением бактерии из в норме стерильных зон однозначно установили роль S. maltophilia как истинного возбудителя.
Хотя S. maltophilia относится к преимущественно нозокомиальным возбудителям, случаи внебольничной инфекции могут случаться чаще, чем это считалось ранее [32]. Наиболее часто встречающимися проявлениями инфекции являются бактериемия, пневмония, инфекция мочевого тракта, инфекция в области хирургического вмешательства и перитонит [108].
Бактериемия
Бактериемия является распространенным проявлением инфекции S. maltophilia и, по всей видимости, частота ее развития у пациентов ОРИТ возрастает [45].
Бактериемия может быть вторичной при первичном источнике инфекции в легких, мочевом и желудочно-кишечном трактах, однако нередко выявить входные ворота не представляется возможным [108]. Публикуется все больше сообщений о значимости устройств для внутривенного введения в патогенезе бактериемии S.
maltophilia и в случаях, когда не установлен явный первичный очаг, предполагается, что именно эти устройства могут быть источником инфекции [113]. Так Muder с соавт. сообщает о том, что в изученной им группе из 91 пациента с бактериемией S.
maltophilia, у 56% не было клинически выявлено входных ворот инфекции, но 84% из этих больных имели установленный центральный венозный катетер [53]. В некоторых случаях было возможно установить резервуар в окружающей среде, из которого S. maltophilia была занесена.
Flaherty с соавторами [23] изучили вспышку грамнегативной бактериемии, включавшую четыре случая, вызванных со S.maltophilia. В качестве источника было установлено О-кольцо в аппарате гемодиализа. В серии случаев, о которых сообщает Fisher с соавт. [22], источником были контаминированные системы мониторинга, используемые во время операции на открытом сердце.
Senol с соавторами сравнили в своем ретроспективном исследовании пациентов с бактериемией, вызванной S.
maltophilia и пациентов группы контроля, подобранных по методу случай-контроль в соответствии с клиническими и демографическими характеристиками.
У пациентов исследуемой группы уровень смертности был значительно выше с уровнем атрибутивной летальности бактериемии S. maltophilia 27,7 % [104].
Jumaa с соавт. также изучали эпидемиологию бактериемии, вызванной S. maltophilia в одном из госпиталей Объединенных Арабских Эмиратов. Все эпизоды бактериемии, связанной со S. maltophilia были внутрибольничными. В большинстве случаев бактериемия была связана с контаминацией катетера и венозной линии. Основными предрасполагающими факторами были злокачественные новообразования [95].
В исследовании Ubeda с соавторами основными сопутствующими факторами при развития бактериемии S. maltophilia были гемобластозы, госпитализация в ОРИТ, предшествующее назначение антибиотиков широкого спектра, имуносупрессия, связанная с использованием кортикостероидов и химиотерапии [113].Сообщается, что уровень смертности у пациентов с бактериемией, связанной со S. maltophilia может составлять от 10 до 60 % [97, 98], она встречается преимущественно у больных в критическом состоянии с тяжелой иммуносупрессией. Однако, атрибутивная летальность, связанная с бактериемией S.
maltophilia, по всей видимости, эквивалента бактериемии, вызванной другими микроорганизмами при сравнении групп, равнозначных по сопутствующим заболевания [97, 104].
Значимыми факторами, ассоциированными с выживаемостью, являются своевременное удаление инфицированного устройства сосудистого доступа и назначение адекватной антибактериальной терапии [116].
В исследовании Lai с соавторами при одномерном анализе данных нозокомиальная бактериемия, длительно сохраняющаяся нейтропения (> 10 дней), бактериемия, связанная с инфекцией респираторного тракта, шок, низкий уровень сывороточного альбумина (
Stenotrophomonas maltophilia
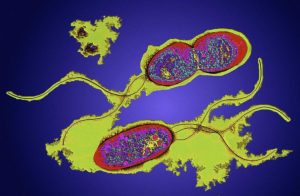
Stenotrophomonas maltophilia в горле что это
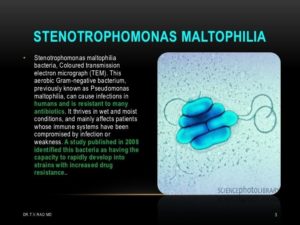
Стенотрофомонас (Stenotrophomonas maltophilia)
Синонимы: Pseudomonas maltophilia или Xanthomonas maltophilia
За последние три десятилетия в связи с интенсивным развитием медицинских технологий и совершенствованием оказания помощи при многих острых критических состояниях и декомпенсации хронических заболеваний, в ОРИТ увеличилось количество ослабленных больных с тяжелым соматическим фоном и инфекционными осложнениями. В свою очередь, в этих условиях, в результате необходимости использования антибиотиков широкого спектра существенно выросла значимость в качестве возбудителей нозокомиальных инфекций слабовирулентных микроорганизмов, обладающих природной резистентностью ко многим антимикробным препаратам.
К таким микроорганизмам относится и Stenotrophomonas maltophilia, неферментирующая грамотрицательная бактерия, ранее известная как Pseudomonas maltophilia или Xanthomonas maltophilia.
До недавнего времени, S. maltophilia считалась достаточно необычным микроорганизмом при выделении в диагностической микробиологической лаборатории. Частота выделения возросла с начала 1970-х годов. Вероятно, такой рост связан с достижениями медицинских технологий в результате чего увеличилось количество пациентов с имеющимися факторами риска развития инфекции.
Сравнение факторов риска между разными исследованиями затруднено из-за разнородности популяции пациентов, критериев, используемых для выявления инфекции и статистических методов, использованных для обработки данных.
Примечательно, однако, что некоторые из них, такие как предшествующее назначение антибактериальных препаратов, связываются с инфекцией S. maltophilia большинством авторов и что почти все факторы риска свидетельствуют о выраженном снижении антиинфекционной защиты пациента.Описано несколько серьезных вспышек инфекции и/или колонизации S. maltophilia. В нескольких случаях был выявлен источник загрязнения. Контаминированная дистиллированная вода, которая использовалась для изготовления дезинфицирующих растворов была установлена в качестве источника одной вспышки инфекции S.
maltophilia, в которую были вовлечены 63 пациента в одном австралийском госпитале. Четыре случая септицемии S. maltophilia были связаны с недостаточной дезинфекцией многоразовых диализаторов.
У восьми пациентов гематологического отделения (четверо с лейкемией и четверо с множественной миеломой) с развившейся инфекцией S. maltophilia, таким источником стала морозильная камера. Лед использовался для создания прохладных напитков и содержал высокую концентрацию бактерий (> 105 КФЕ/мл).
Этиология и патогенез [ править ]
Stenotrophomonas maltophilia — единственный представитель рода Stenotrophomonas (Stenos, греч. — узкий; trophos, греч. — питающаяся; monas, греч. — единица, организм; и malt, староанглийский — солод; philos, греч.- друг).
Название отражает ограниченную способность вида использовать питательные субстраты при способности образовывать кислые продукты из мальтозы («солодовый сахар»), что было использовано при разработке среды для селекции S. maltophilia.
Род был выделен в 1993 году Palleroni и Bradbury после многолетних дебатов относительно таксономического положения этого микроорганизма.
Клетки S. maltophilia прямой или слегка изогнутой формы неспорообразующие грамотрицательные бациллы, от 0,5 до 1,5 мкм длиной. Они подвижны, благодаря наличию нескольких полярно расположенных жгутиков. Колонии гладкие, блестящие с ровными краями, белого или бледно-желтого цвета. S. maltophilia облигатный аэроб.
Рост не отмечается при температуре выше 40° С и ниже 5°. Оптимальная температура для роста — 35° С. Бактерия относится к относительно метаболически неактивным микроорганизмам, но может метаболизировать ряд необычных субстратов, включая аминогликозидный антибиотик стрептомицин.
Штаммы бактерии изучаются для потенциального использования в качестве биодеградантных агентов.
Stenotrophomonas maltophilia широко распространена в окружающей среде и географических регионах, включая Антарктику, и занимает экологические ниши как внутри так и за пределами больниц.
Бактерия была выделена из большого количества нозокомиальных источников, включая контуры аппаратов искусственной вентиляции, руки персонала, аппараты диализа, небулайзеры, устройства для ингаляционной терапии и даже растворы дезинфектантов. Достаточно мало информации известно о способности S.
maltophilia переносить высушивание, однако Rosenthal сообщает, что хотя бактерия достаточно часто выделяется во влажной среде, обнаружение ее в сухих местах, таких как больничный пол, встречается нечасто.О факторах вирулентности S. maltophilia известно мало. Сложности с разделением колонизации и инфекции привело к формированию представления об ограниченной патогенности возбудителя. Описана выработка бактерией ряда внеклеточных ферментов, включая ДНКазу, РНКазу, фибринолизин, липазу, гиалуронидазу, протеазу и эластазу.
Сродство к пластику считается важным свойством бактерии, часто формирующей колонизацию и инфекцию вдоль инфузионных линий и внутривенных канюль. Способность S. maltophilia выживать и размножаться в растворах для парентерального питания и других типах инфузионных сред может также вносить вклад в патогенез ассоциированных с внутривенной линией инфекций.
Также известна способность бактерии к росту в диализных растворах с высвобождением низкомолекулярных пирогенов.
Клинические проявления [ править ]
Спектр клинических проявлений, связанных с инфекцией Stenotrophomonas maltophilia постоянно расширяется. Многие ранние публикации не могли установить четкие признаки инфекции, связанной с этим микроорганизмом.
Действительно, частое выделение бактерий в смешанных культурах, трудность разделения инфекции и колонизации в области поверхностных зон, таких как кожа или верхние отделы дыхательных путей сформировали мнение, встречающееся в ранних публикациях, о том, что S. maltophilia является организмом со строго ограниченным патогенным потенциалом.
Однако, более поздние исследования, в которых использовались строгие критерии определения инфекции, связанной с выделением бактерии из в норме стерильных зон однозначно установили роль S. maltophilia как истинного возбудителя.
Хотя Stenotrophomonas maltophilia относится к преимущественно нозокомиальным возбудителям, случаи внебольничной инфекции могут случаться чаще, чем это считалось ранее. Наиболее часто встречающимися проявлениями инфекции являются бактериемия, пневмония, инфекция мочевого тракта, инфекция в области хирургического вмешательства и перитонит.
Pseudomonas (aeruginosa) (mallei) (pseudomallei): Диагностика [ править ]
Основной метод — бактериологический. Материал для исследования — кровь, мокрота, моча, раневое отделяемое, спиномозговая жидкость. Возможна идентификация путем хроматографического анализа клеточных жирных кислот.
Pseudomonas (aeruginosa) (mallei) (pseudomallei): Лечение [ править ]
Инфекции, вызванные S. maltophilia очень трудно контролировать , потому что клинические изоляты часто резистентны ко многим антимкробным препаратам.
Дополнительные сложности связаны с методологией проведения тестов чувствительности.
Методы дисковой диффузии, по всей видимости, не точен и плохо воспроизводим, с существенной вариабельностью результатов при оценке диаметра зоны после 24 и 48 часов инкубации.
Национальный Комитет по Клиническим Лабораторным Стандартам США (NCCLs) рекомендует использовать тесты по изучению минимальной подавляющей концентрации в агаре или методы разведения в бульоне. Использование традиционного и широко распространенного в практике метода дисковой диффузии не рекомендуется.
Выбор препарата для терапии инфекций, обусловленных S. maltophilia представляет собой сложную задачу, как для клиницистов, так и для микробиологической лаборатории.
За некоторым исключением, в большинстве исследований было установлено, что триметоприм-сульфаметоксазол был активен против большей части штаммов микроорганизма и этот препарат в течение длительного времени считается препаратом выбора для лечения инфекции S. maltophilia, не смотря на его бактериостатические свойства в отношении большинства изолятов.
Учитывая последнее обстоятельство, некоторые авторы рекомендуют назначать препарат в максимально переносимых дозах. Токсичность сульфаниламидного компонента комбинированного препарата может быть ограничивающим фактором в этом контексте.Высокие дозы особенно плохо переносятся пациентами старшего возраста со сниженной функцией почек из-за возможных тяжелых кожных реакций, миелосупрессии и тромбоцитопении. Пенициллины и цефалоспорины за редким исключением проявляет плохую активность в отношении S. maltophilia.
Резистентность бактерии к карбапенемам, включая новые препараты класса, такие как биапенем, хорошо известна, хотя отмечается широкая вариация результатов чувствительности. Цефтазидим, по- видимому, проявляет наиболее высокую активность среди цефалоспоринов, но результаты чувствительности к нему широко варьируют, и препарат не может быть рекомендован для эмпирической терапии.
Чувствительность микроорганизма к представителям ранних фторхинолонов, таких как ципрофлоксацин, значительно варьирует, но имеются отдельные сообщения об эффективной терапии этими препаратами при системной инфекции S. maltophilia. Однако отмечалась также и суперинфекция S.
maltophilia на фоне терапии фторхинолонами и случаи неэффективности терапии этими препаратами , поэтому использовать эти препараты для эмпирической терапии нужно с осторожностью. Новые фторхинолоны, такие, как клинафлоксацин, тровафлоксацин, левофлоксацин и моксифлоксацин по всей видимости, более эффективны в отношении бактерии, чем препараты ранних генераций.
Хотя данные чувствительности in vitro кажутся многообещающими, к настоящему времени имеется мало сведений по использованию новых фторхинолонов в клинической практике, и результаты клинических исследований ожидаются с большим интересом. Активность аминогликозидов, включая новейшие препараты этого класса, такие как изепамицин против S.
maltophilia не высока и эти препараты в общем имеют ограниченное значение при монотерапии. In vitro наблюдался синергизм аминогликозидов с другими антимикробными препаратами. Монотерапия при ведении инфекции S.
maltophilia часто дает неудовлетворительные результаты, поэтому не удивительно, что многие исследователи предлагают использовать комбинацию антибактериальных препаратов и пытаются выявить препараты, которые обладают синергизмом в отношении бактерии in vitro.Комбинированная терапия может быть назначена пациентам с тяжелыми заболеваниями, плохим клиническим ответом на предыдущую терапию или тем, у которых микроорганизм in vitro проявляет резистентность ко всем тестируемым препаратам. Muder с соавторами установили, что комбинация триметоприм-сульфаметоксазола с тикарциллин-клавуланатом или цефалоспоринами расширенного спектра может быть более эффективна, чем монотерапия. У пациентов с аллергией к пенициллинам, можно использовать комбинацию ко-тримоксазола и ципрофлоксацина. Пациентам с аллергией к триметоприм-сульфаметоксазолу необходимо рассмотреть возможность десенситизации к этому препарату либо назначения комбинации тикарциллин-клавуланата с ципрофлоксацином. Подбирать антимикробную терапию при лечении инфекции, связанной со S. maltophilia следует большой осторожностью, поскольку она очень часто сочетается с инфекцией, вызванными другими микроорганизмами. В этой связи, ограничение терапии препаратами, активными только в отношении S. maltophilia опасно, так как типичные возбудители могут быть резистентными к триметоприм/сульфаметоксазолу.
Вас заинтересует: Герпетическая инфекция горла у ребенка чем лечить
Прочее [ править ]
Синонимы: Pseudomonas aeruginosa
Синегнойная палочка сапрофитирует на коже человека, чаще в местах, где развиты потовые железы. Является одним из возбудителей внутрибольничной инфекции в ожоговых отделениях и отделениях интенсивной терапии.
Развивается при пониженной сопротивляемости организма.
Подавляет регенерацию тканей, обладает высокой устойчивостью к антибиотикам и химическим антисептикам (кроме полимиксина, амикацина, карбенициллина, борной кислоты).
Источники (ссылки) [ править ]
Зубарев А.С. «Инфекции, связанные со Stenotrophomonas maltophilia у пациентов отделений реанимации и интенсивной терапии» Журнал «Интенсивная терапия» N1 — 2008
Общая хирургия [Электронный ресурс]: учебник / В. К. Гостищев. — 5-е изд., перераб. и доп. — М. : ГЭОТАР-Медиа, 2015.
источник
