Обнаружили acinetobacter baumannii
Вирусы вместо антибиотиков. Как бороться с суперинфекциями
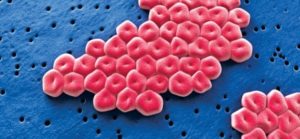
МОСКВА, 11 апр — РИА Новости, Альфия Еникеева. С некоторых пор болезнетворные бактерии стали вырабатывать устойчивость к антибиотику последнего резерва — колистину.
Его применяют в тех случаях, когда остальные лекарства бессильны перед возбудителями инфекций.
Неубиваемые микроорганизмы появились даже в Арктике, а Всемирная организация здравоохранения составила список из 12 наиболее опасных супербактерий, средство против которых необходимо найти уже сейчас.
Глобальная угроза
По данным британских исследователей, к 2050 году число смертей от антибиотикорезистентных супербактерий с сегодняшних семисот тысяч увеличится до десяти миллионов в год.
Чаще всего люди, как считают специалисты ВОЗ, будут умирать от устойчивых к карбапенему энтеробактерий, синегнойной палочки (Pseudomonas aeruginosa) и ацинетобактера (Acinetobacter baumannii).
Все эти возбудители связаны с так называемыми внутрибольничными инфекциями, которые пациенты цепляют в госпиталях и поликлиниках, где лечатся от других заболеваний.
Также среди наиболее опасных супербактерий, по данным ВОЗ, оказались энтерококки (Enterococcus faecium), золотистый стафилококк (MRSA), гонококк и устойчивый к кларитромицину хеликобактер — патогены, вызывающие менингит, заражение крови, пневмонию, гонорею и инфекции мочевыводящих путей.
Судя по эксперименту гарвардских ученых, невосприимчивость к лекарствам развивается у этих микроорганизмов стремительно. Обычная кишечная палочка Escherichia coli всего за 11 дней приспособилась к тысячекратной дозе антибиотиков и фактически превратилась в супермикроб, практически неуязвимый для любых существующих препаратов.
Найти новый антибиотик
Теоретически ученые способны создать лекарство против бактерий, нечувствительных к нынешним антибиотикам, однако его разработка и испытания могут занять долгие годы. А это, в свою очередь, может быть финансово невыгодно фармацевтическим компаниям.
Выход из сложившейся ситуации предложили исследователи из МФТИ, МГУ и Института биохимии и генетики РАН, придумавшие полуавтоматический метод поиска антибиотиков нового класса. Он основан на анализе того, как те или иные вещества действуют на патогенные микроорганизмы и уничтожают их.
Ученые проверили действие почти 125 тысяч соединений на штамме кишечной палочки Escherichia coli и выявили 688 веществ, обладающих выраженной антибактериальной активностью. Некоторые из них обладали одинаковой подструктурной 2-пиразол-1-ил-тиазол группой.
А значит, соединения, относящиеся к этому классу, могут быть эффективны в борьбе с лекарственно устойчивыми бактериями.
Затем исследователи проанализировали принадлежащие к этой группе восемь молекул, которые уничтожали микроорганизмы, блокируя им синтез белка. Среди изученных веществ только одно не проявляло цитотоксического эффекта и гипотетически не представляло опасности для человека. Однако его еще следует тщательно исследовать и испытывать на модельных животных, отмечают авторы работы.
Вирусы против бактерий
Американские ученые предлагают бороться с микроорганизмами, устойчивыми к антибиотикам, с помощью бактериофагов — вирусов, избирательно поражающих бактериальные клетки. Правда, при такой терапии следует использовать частицы, созданные специально под определенный штамм возбудителя.
Специалисты уже помогли подобным образом пациентке, страдающей муковисцидозом и хронически инфицированной антибиотикорезистентным штаммом Mycobacterium abscessus. В начале 2018 года девушке провели двустороннюю трансплантацию легких, а потом обнаружили в анализах опасную микобактерию, спровоцировавшую загноение послеоперационной раны.
Противомикробная терапия в течение семи месяцев не давала никаких результатов.
Тогда ученые подобрали три фага, наиболее агрессивных по отношению к патогенному микроорганизму, смешали их и проверили действие созданного препарата на культуре штамма GD01 Mycobacterium abscessus, который был выделен у пациентки через месяц после операции. Полученная смесь не оставляла в живых ни одной бактерии, даже при высоких концентрациях.
Затем комбинацию из трех бактериофагов в течение 32 недель внутривенно вводили пациентке каждые 12 часов. В результате ее состояние значительно улучшилось: послеоперационная рана стала заживать, а опасная бактерия больше не проявлялась в мокроте и крови.
Впрочем, авторы статьи предупреждают: говорить об эффективности лечения бактериофагами пока рано, ведь это единичный клинический случай. Тем не менее в медицинской литературе уже описана успешная терапия инфекций, вызванных супербактериями, с помощью антибиотиков и бактериофага.
Искусственные и эффективные
Китайские, американские и сингапурские ученые синтезировали вещество, способное разрушить сразу несколько бактерий, устойчивых к антибиотикам, — в том числе синегнойную палочку и золотистый стафилококк (MRSA).
Речь идет о биоразлагаемом поликарбонатном полимере с гуанидиновыми функциональными группами, чьи молекулы могут связываться с бактериальной мембраной и, не разрушая ее, проникать внутрь клетки. Там гуанидин нарушает структуру белков цитоплазмы, и они выпадают в осадок, убивая бактерию.
Исследователи протестировали новое лекарство на крысиных эритроцитах и клетках эмбриональных человеческих почек. Полимер оказался абсолютно нетоксичен для первых и менее ядовит для вторых, чем антибиотик полимиксин В, используемый сегодня в лечении бактериальных инфекций.
Кроме того, новое соединение полностью разлагалось за трое суток, а продукты его распада были безвредны.
Кроме того, выяснилось, что созданный учеными полимер не вызывает привыкания у опасных микроорганизмов. Специалисты обрабатывали культуру Acinetobacter baumannii — возбудителя пневмонии — этим соединением в концентрациях, позволявших некоторым бактериям выживать.
Затем из них выращивали новую культуру и снова обрабатывали ее поликарбонатом. И так тридцать раз подряд. Однако даже после этого микробы не выработали устойчивости к полимеру.Для сравнения: резистентность к антибиотику, который обычно применяют против Acinetobacter baumannii, бактерии выработали за восемь циклов.
Авторы работы намерены в будущем протестировать созданный ими полимер на людях.
Acinetobacter lwoffii лечение
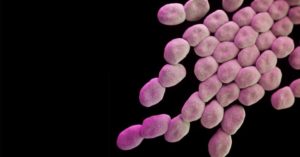
- Acinetobacter baumannii
- Pseudomonas aeruginosa
- Enterobacteriaceae
бактерий, устойчивых к антибиотикам, заслуженно возглавляют грамотрицательные микроорганизмы — возбудители большинства нозокомиальных (внутрибольничных) инфекций в отделениях реанимации и интенсивной терапии, гнойной хирургии и онкологии. Вызывают инфекции кожи и мягких тканей, ЖКТ, мочевыводящих путей, раневые, эндокардит, менингит, остеомиелит.
«Природное» местообитание A. baumannii не установлено, однако этих бактерий обнаруживают в стационарах по всему миру. Вызывает до 1 % всех нозокомиальных инфекций, с уровнем смертности от 8 до 35 %.
A. baumannii резистентна к пенициллинам, цефалоспоринам, аминогликозидам, хинолонам и тетрациклину. Отмечено значительное увеличение резистентности к карбапенемам — более 50 % в отдельных странах.
https://www..com/watch?v=upload
В терапии карбапенем-резистентной A. baumannii относительно эффективны комбинации антибиотиков: полимиксин Е рифампицин/карбапенемы/хинолоны/цефепим/ампициллин-сульбактам/пиперациллин-тазобактам.
Синегнойная палочка распространена повсеместно, встречается в почве и воде, на/в растениях, животных, людях. Вызывает до 20 % нозокомиальных инфекций. Чувствительность к антибактериальной терапии очень сильно варьирует.
В тяжелых случаях отмечается развитие резистентности к ранее высокоэффективным цефалоспоринам, фторхинолонам, карбапенемам, аминогликозидам, азтреонаму, пиперациллину-тазобактаму.
Сохраняется чувствительность к полимиксину Е, а также комбинациям антибиотиков.
Смертность при развитии инфекций, вызванных мультирезистентной P. aeruginosa, варьирует от 5 до 50 %, в зависимости от состояния пациента и локализации процесса.
Enterobacteriaceae
Из большого семейства энтеробактерий основные проблемы в стационарах доставляют Klebsiella, Escherichia coli, Citrobacter, Salmonella, Enterobacter, Serratia, Proteus. Вызывает опасения растущее повсеместное снижение чувствительности семейства к карбапенемам. Описаны единичные случаи резистентности E. coli ко всем существующим антибиотикам, включая полимиксин Е.
- Enterococcus faecium
- Staphylococcus aureus
- Helicobacter pylori
- Campylobacter spp.
- Salmonellae
- Neisseria gonorrhoeae
Бактерии второй группы объединены по признаку повсеместного распространения, высокой социально-экономической значимости вызываемых ими заболеваний и быстрого развития резистентности к основным антибиотикам, используемым для их эрадикации, однако в резерве еще остается один или несколько эффективных препаратов.
E. faecium входит в состав нормальной микрофлоры кишечника, но в то же время является условно-патогенным микроорганизмом. У ослабленных больных может вызывать инфекции мочевыводящих путей, раневую инфекцию, сепсис и эндокардит.
Резистентен к аминогликозидам, пенициллинам и цефалоспоринам. Беспокойство вызывает снижение чувствительности к ванкомицину — до 72 % в отдельных популяциях. Большинство штаммов E.
faecium чувствительны к линезолиду, тигециклину, даптомицину.
Золотистый стафилококк, колонизирующий кожу и слизистые оболочки, способен вызывать тяжелые инфекции кожи и мягких тканей, респираторные, раневые инфекции, остеомиелит, сепсис, артрит, эндокардит. Недавнее появление и распространение ванкомицин- и гликопептид-резистентных штаммов в дополнение метициллин-резистентному S.
Helicobacter pylori
Тревогу ВОЗ вызывает увеличение случаев резистентности всем известной H. pylori к кларитромицину, что сказывается на эффективности традиционных схем эрадикационной терапии, в том числе и в России.
Перед эрадикацией ВОЗ рекомендует проверить чувствительность бактерии к этому антибиотику, при выявлении устойчивости — использовать схемы без него — с метронидазолом, тетрациклином или рифаксимином, а также добавлять висмута трикалия дицитрат.
Campylobacter spp
Бактерии рода Campylobacter удерживают первое место в мире по гастроэнтеритам, которые у большинства населения планеты протекают в легкой форме, но представляют опасность для маленьких детей, беременных, стариков и иммунокомпрометированных больных. В большинстве случаев достаточно регидратации и восстановления электролитного баланса, антибактериальную терапию назначают при тяжелом течении.
Проблемой является резистентность Campylobacter к фторхинолонам, основному средству борьбы с кишечной микрофлорой, и макролидам. Устойчивость к этим препаратам, впрочем, сильно варьирует от страны к стране — от менее 5 % в Финляндии до более 90 % в Индии. В Европе и России эритромицин всё еще остается препаратом выбора.
Salmonellae
Представители рода сальмонелл также вызывают набор кишечных инфекций, от легкого энтерита до брюшного тифа. Большинство этих бактерий уже резистентны к бета-лактамам, аминогликозидам, тетрациклинам, хлорамфениколу и ко-тримоксазолу.
Устойчивость к фторхинолонам растет во всем мире, но пока не привела к полной бесполезности этих препаратов, они остаются антибиотиками выбора, наравне с макролидами и цефалоспоринами третьего поколения.
Антибактериальной терапии требуют только тяжелые случаи кишечных инфекций и, конечно, брюшной тиф и паратифы.
Гонорея из неприятной, но относительно легко излечимой болезни эволюционировала в глобальную медицинскую проблему. Гонококк потерял чувствительность к пенициллинам, тетрациклинам, сульфаниламидам и фторхинолонам.Особое опасение вызывает появление и постепенное распространение штаммов, резистентных к цефалоспоринам (цефтриаксону), долгое время служивших безотказным средством борьбы с этой инфекцией.
При резистентной к стандартным схемам лечения гонорее рекомендовано использовать комбинацию азитромицина с высокими дозами цефтриаксона.В России гонококк также практически резистентен к фторхинолонам, но пока сохраняет 100 %-ную чувствительность к цефтриаксону.
Средний уровень приоритетности
- Streptococcus pneumoniae
- Haemophilus influenzae
- Shigella spp.
Третью группу также представляют широко распространенные бактерии, чья устойчивость к «обычным» антибиотикам пока не приняла угрожающих масштабов, однако чревата большими проблемами в будущем.
Пневмококки — одни из основных возбудителей инфекций ЛОР-органов, внебольничной пневмонии, менингита. Резистентны к тетрациклину и ко-тримоксазолу. В мире постепенно снижается чувствительность S. pneumoniae к бета-лактамам и макролидам, однако, как и в других случаях, доля резистентных штаммов сильно варьирует от страны к стране.
Гемофильная инфекция у детей младшего возраста протекает в виде бактериемии, гнойного менингита, пневмонии, целлюлита и эпиглоттита, у взрослых — в основном в виде пневмонии.
Тревогу ВОЗ вызывает развитие полной резистентности гемофильной палочки к ранее эффективному ампициллину, в результате чего от него пришлось повсеместно отказаться.
В России эффективны амоксициллин, цефалоспорины и макролиды, однако рекомендуется проводить бактериологический анализ с оценкой резистентности.
Shigella spp
Возбудители дизентерии практически не чувствительны к ампициллину. Как и прочие энтеробактерии, они также постепенно вырабатывают устойчивость к фторхинолонам, которые тем не менее всё еще остаются препаратами выбора. В качестве альтернативы — цефалоспорины III поколения, ко-тримоксазол.
Итого
Появление устойчивых к антибиотикам бактерий и публикация этого списка в очередной раз привлекают внимание человечества к необходимости создания — в идеале — принципиально новых средств борьбы с микроорганизмами, иначе, по пессимистичным прогнозам, из-за появления бактерий, устойчивых к антибиотикам, через несколько десятилетий одна только послеоперационная летальность может скатиться до уровня начала прошлого века.
https://www..com/watch?v=ytpolicyandsafetyru
Проблема лекарственной устойчивости среди возбудителей нозокомиальных инфекций — первые пять бактерий списка — актуальна и для российского здравоохранения.
Остальные перечисленные микроорганизмы, по данным российских исследований, на территории РФ в целом сохраняют чувствительность к «своим» антибиотикам.
Тем не менее, учитывая возросшую мобильность населения, можно ожидать завоза и распространения резистентных штаммов.Сводная таблица: чувствительность возбудителей к антибактериальной терапии
| Возбудитель | Чувствительность к антибактериальной терапии | ||
| Нет или в большинстве случаев утеряна | Снижается | В основном сохранена | |
| Acinetobacter baumannii | Пенициллины, цефалоспорины, аминогликозиды, тетрациклин, хинолоны, азтреонам, пиперациллин-тазобактам | Карбапенемы, полимиксин Е | Комбинации:полимиксин Е рифампицин/карбапенемы/хинолоны/цефепим/ампициллин-сульбактам/пиперациллин-тазобактам |
Характеристики Acinetobacter baumannii, морфология, обмен веществ / биология
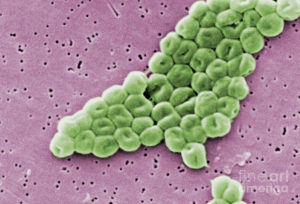
Acinetobacter baumannii Это грамотрицательная бактерия, принадлежащая к отряду псевдомонад. На протяжении всей своей таксономической истории он находился в Micrococcus, Moraxella, Alcaligenes, Mirococcuscalco-aceticus, Herellea и Achromobacter, пока он не был расположен в своем нынешнем жанре в 1968 году.
. baumannii Это патогенная бактерия, которая считается видом, наиболее часто встречающимся в инфекциях своего рода. Она была замешана в различных типах инфекций, таких как сепсис, пневмония и менингит..
Это оппортунистический паразит, который часто встречается в больничных или внутрибольничных заболеваниях. Передача через искусственную вентиляцию легких была указана как важная причина инфекции, особенно в отделениях интенсивной терапии.
Несмотря на то, что он считается низкосортным патогеном, он обладает способностью увеличивать свою вирулентность у штаммов, вовлеченных в частые инфекции. Обладает большой способностью развивать резистентность и мультирезистентность к антибиотикам..
В больницах он передается в основном через контакт с персоналом, через загрязненные больничные материалы, а также через воздух на короткие расстояния..
Всемирная организация здравоохранения включает А. Бауманны в списке устойчивых патогенов, для которых срочно требуются новые антибиотики, с присвоением категории 1 с критическим приоритетом.
индекс
- 1 Биологические характеристики
- 2 Морфология
- 3 Метаболизм
- 4 Устойчивость к антибиотикам
- 5 патологий
- 6 Симптомы
- 7 Лечение
- 8 ссылок
Биологические характеристики
Все виды рода Acinetobacter они имеют широкое распространение в разных природных нишах. А. Бауманны он может естественным образом обитать на коже здоровых людей, будучи способен колонизировать слизистые поверхности, что является важным эпидемиологическим резервуаром. Тем не менее, среда обитания А. Бауманны это почти исключительно для больниц.
Эти бактерии не имеют жгутики или структуры, используемые для передвижения. Однако движение достигается за счет структур, которые позволяют им расширить и втягиваться, а также химических механизмов, таких, как выведение пленки с высокой молекулярной массой, экзополисахарида позади бактерий.
А. Бауманны может колонизировать большое количество живых или инертных сред и обладает большой способностью выживать на искусственных поверхностях в течение длительного периода времени.
Эта способность, возможно, из-за его способность противостоять обезвоживанию, используя различные источники углерода через различные метаболические пути и способность образовывать биопленки. По этой причине он является общим, чтобы найти его в больничных принадлежностей, таких как катетеры и механической вентиляции устройства.
морфология
A. baumannii — коккобацилл, промежуточный по форме между кокосами и тростниками. Они измеряют от 1,5 до 2,5 на 1-1,5 мкм, когда популяции находятся в логарифмической фазе роста. Они более сферические, когда достигают стационарной фазы.
метаболизм
Бактерия А. Бауманны это не ферментер глюкозы; он строго аэробный, то есть для метаболизма необходим кислород.
Вид рода Acinetobacter они являются единственными из семейства Moraxellaceae, в которых отсутствуют оксидазы цитохрома с, для которых они дают отрицательные результаты в тестах оксидаз.
А. Бауманны растет при температуре от 20 до 44ºC, оптимальная температура от 30 до 35ºC.
Устойчивость к антибиотикам
Постоянная генерация устойчивости к антибиотикам не только препятствует лечению инфекций, вызываемых А. Бауманны, это также способствует отбору эндемических и эпидемических мультирезистентных штаммов.
Некоторые внутренние механизмы А. Бауманны, которые способствуют устойчивости к антибиотикам:
- Наличие β-лактамазы придают устойчивость к b-лактамам.
- Продукция специфических ферментов, таких как аммониглюкозид-3'-фосфотрансфераза VI, инактивирует амикацин.
- Присутствие оксациллиназы ОХА-51 гидролизует пенициллины и карбапенемы.
- Присутствие и избыточная экспрессия эффлюксных наркотиков насосов, которые являются насосами, которые высылать вне клетки к малым молекулам, которые способны ввести в цитоплазму, снижающие чувствительность к антибиотикам.
Биопленки, созданные А. Бауманны они изменяют метаболизм микроорганизмов, снижая их чувствительность к антибиотикам, а также создают физический барьер против больших молекул и предотвращают обезвоживание бактерий..
патологиями
А. Бауманны колонизирует нового хозяина путем контакта с инфицированными людьми или с загрязненным медицинским оборудованием. Во-первых, эта бактерия прилипает к поверхности кожи и слизистой оболочки. Для размножения необходимо выжить антибиотики и ингибиторы и условия этих поверхностей.
Увеличение числа бактерий на поверхности слизистых оболочек, в частности в стационарных катетеров контакта внутрисосудистых или эндотрахеальных трубок, может повысить риск инфекции дыхательных путей и кровоток.
Пневмония в больницах является наиболее распространенной из инфекций, вызываемых А. Баумании. Обычно заключаются в отделениях интенсивной терапии пациентами, получающими искусственное дыхание.
А. Баумании Это также вызвало серьезные проблемы из-за заражения военнослужащих послевоенными травмами, особенно в Ираке и Афганистане. В частности, из-за остеомиелита и инфекций мягких тканей, которые могут вызвать некроз и целлюлит.
Есть также риск менингита от А. Баумании у пациентов, восстанавливающихся после нейрохирургии.
Лица, подверженные заражению А. Баумании включают в себя те, которые были ранее подвергнуты антибиотикам, серьезной операции, ожоги, травмы, иммуносупрессии или использования инвазивных медицинских устройств, в первую очередь для искусственной вентиляции легких в отделениях интенсивной терапии.
симптомы
Не существует специфической симптоматики инфекций из-за А. Баумании. Каждая из различных инфекций, вызываемых этой бактерией, имеет свои характерные симптомы.
В целом симптомы инфекций, которые могут включать А. Баумании или другие оппортунистические бактерии, такие как Klebsiella pneumoniae и Streptococcus pneumoniae, Они могут включать лихорадку, озноб, сыпь, болезненное мочеиспускание, насущную необходимость часто мочиться, путаницы или измененных психических состояний, тошнота, боли в мышцах, груди и кашель.
лечение
Антибиотики для лечения инфекций А. Бауманны они чрезвычайно ограничены из-за их большой способности приобретать сопротивления и мультирезистентность. Поэтому важно определить восприимчивость каждого штамма к различным антибиотикам, чтобы обеспечить эффективность каждого лечения..
В связи с устойчивостью к карбапенемам использовалось использование полимиксинов, в частности колистина, несмотря на относительно низкий индекс резистентности и его побочные эффекты на почки..
Однако штаммы, устойчивые к колистину, уже были обнаружены. В качестве альтернативы устойчивости к этим антибиотикам использовалась комбинированная терапия..
ссылки
- Bergogne-Bérézin, E. & Towner, K.J. Acinetobacter spp. как внутрибольничные патогены: микробиологические, клинические и эпидемиологические особенности. Clin Microbiol Rev, 9 (1996), pp. 148-165.
- Fournier, P.E., Richet, H. (2006). Эпидемиология и контроль Acinetobacter baumanii в учреждениях здравоохранения. Клинические инфекционные заболевания, 42: 692-9.
- Эрнандес Торрес, А., Гарсия Васкес, Е., Ягуэ, Г. &, Гомес Гомес, J. (2010) Acinetobacter baumanii мультирезистентность: текущая клиническая ситуация и новые перспективы Испанский журнал химиотерапии, 23 (1): 12-19.
- Марагакис Л.Л., Perl TM. Acinetobacter baumanii: эпидемиология, устойчивость к противомикробным препаратам и варианты лечения. Clin Infec Dis 2008; 46: 1254-63.
- McConnell, M.j., Actis, L. & Pachón, J. (2013) Acinetobacter baumannii: инфекции человека, факторы, способствующие патогенезу и модели на животных. FEMS Microbiology Reviews, 37: 130-155.
- Peleg, A.Y., Seifert, H. & Paterson, D.L. (2008). Acinetobacter baumannii: появление успешного возбудителя. Клиническая Микробиология Обзоры, 21 (3): 538-82.
- Ванегас-Мунера, J.M., Roncancio-Villamil, G. & Jiménez-Quiceno, J.N. (2014). Acinetobacter baumannii: клиническое значение, механизмы резистентности и диагностика. CES Medicine Journal, 28 (2): 233-246.
Проклятая дюжина
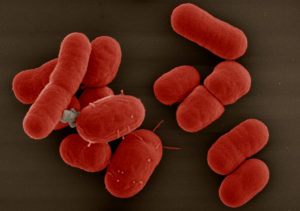
Опубликован список из 12 бактерий, устойчивых к действию большинства антибиотиков
В конце февраля 2017 г. Всемирная организация здравоохранения впервые опубликовала список бактерий с уже выработанной или растущей устойчивостью к действию большинства антибиотиков.
Задача публикации — стимулировать на государственном уровне поиск новых лекарственных препаратов против перечисленных возбудителей, «представляющих наибольшую угрозу для здоровья человека».
Включенные в список бактерии разделены на три группы по приоритетности в плане поиска новых антибиотиков.
Критически высокий уровень приоритетности
- Acinetobacter baumannii
- Pseudomonas aeruginosa
- Enterobacteriaceae
бактерий, устойчивых к антибиотикам, заслуженно возглавляют грамотрицательные микроорганизмы — возбудители большинства нозокомиальных (внутрибольничных) инфекций в отделениях реанимации и интенсивной терапии, гнойной хирургии и онкологии. Вызывают инфекции кожи и мягких тканей, ЖКТ, мочевыводящих путей, раневые, эндокардит, менингит, остеомиелит. У ослабленных пациентов особое значение имеют инфекции кровотока и ИВЛ-ассоциированная пневмония. Для бактерий этой группы практически не осталось антибиотиков резерва.
Acinetobacter baumannii
«Природное» местообитание A. baumannii не установлено, однако этих бактерий обнаруживают в стационарах по всему миру. Вызывает до 1 % всех нозокомиальных инфекций, с уровнем смертности от 8 до 35 %. A.
baumannii резистентна к пенициллинам, цефалоспоринам, аминогликозидам, хинолонам и тетрациклину. Отмечено значительное увеличение резистентности к карбапенемам — более 50 % в отдельных странах.
Выявлены случаи резистентности к «последнему резерву» антибактериальной терапии, полимиксинам, ранее широко не использовавшимся из‑за высокой нефротоксичности.
В терапии карбапенем-резистентной A. baumannii относительно эффективны комбинации антибиотиков: полимиксин Е + рифампицин/карбапенемы/хинолоны/цефепим/ампициллин-сульбактам/пиперациллин-тазобактам.
Pseudomonas aeruginosa
Синегнойная палочка распространена повсеместно, встречается в почве и воде, на/в растениях, животных, людях. Вызывает до 20 % нозокомиальных инфекций. Чувствительность к антибактериальной терапии очень сильно варьирует.
В тяжелых случаях отмечается развитие резистентности к ранее высокоэффективным цефалоспоринам, фторхинолонам, карбапенемам, аминогликозидам, азтреонаму, пиперациллину-тазобактаму.
Сохраняется чувствительность к полимиксину Е, а также комбинациям антибиотиков.
Смертность при развитии инфекций, вызванных мультирезистентной P. aeruginosa, варьирует от 5 до 50 %, в зависимости от состояния пациента и локализации процесса.
Высокий уровень приоритетности
- Enterococcus faecium
- Staphylococcus aureus
- Helicobacter pylori
- Campylobacter spp.
- Salmonellae
- Neisseria gonorrhoeae
Бактерии второй группы объединены по признаку повсеместного распространения, высокой социально-экономической значимости вызываемых ими заболеваний и быстрого развития резистентности к основным антибиотикам, используемым для их эрадикации, однако в резерве еще остается один или несколько эффективных препаратов.
Enterococcus faecium
E. faecium входит в состав нормальной микрофлоры кишечника, но в то же время является условно-патогенным микроорганизмом. У ослабленных больных может вызывать инфекции мочевыводящих путей, раневую инфекцию, сепсис и эндокардит.
Резистентен к аминогликозидам, пенициллинам и цефалоспоринам. Беспокойство вызывает снижение чувствительности к ванкомицину — до 72 % в отдельных популяциях. Большинство штаммов E.
faecium чувствительны к линезолиду, тигециклину, даптомицину.
Staphylococcus aureus
Золотистый стафилококк, колонизирующий кожу и слизистые оболочки, способен вызывать тяжелые инфекции кожи и мягких тканей, респираторные, раневые инфекции, остеомиелит, сепсис, артрит, эндокардит.
Недавнее появление и распространение ванкомицин- и гликопептид-резистентных штаммов в дополнение метициллин-резистентному S.
aureus значительно сужает выбор антибактериальных препаратов, однако у возбудителя сохраняется чувствительность к аминогликозидам, эритромицину, тетрациклину, ко-тримоксазолу, линезолиду.
Neisseria gonorrhoeae
Гонорея из неприятной, но относительно легко излечимой болезни эволюционировала в глобальную медицинскую проблему. Гонококк потерял чувствительность к пенициллинам, тетрациклинам, сульфаниламидам и фторхинолонам.Особое опасение вызывает появление и постепенное распространение штаммов, резистентных к цефалоспоринам (цефтриаксону), долгое время служивших безотказным средством борьбы с этой инфекцией.
При резистентной к стандартным схемам лечения гонорее рекомендовано использовать комбинацию азитромицина с высокими дозами цефтриаксона.В России гонококк также практически резистентен к фторхинолонам, но пока сохраняет 100 %-ную чувствительность к цефтриаксону.
Streptococcus pneumoniae
Пневмококки — одни из основных возбудителей инфекций ЛОР-органов, внебольничной пневмонии, менингита. Резистентны к тетрациклину и ко-тримоксазолу. В мире постепенно снижается чувствительность S.
pneumoniae к бета-лактамам и макролидам, однако, как и в других случаях, доля резистентных штаммов сильно варьирует от страны к стране.
В России большинство штаммов пневмококков, к счастью, всё еще чувствительны к пенициллинам и макролидам, также эффективны хлорамфеникол, рифампицин, левофлоксацин, ванкомицин.
Haemophilus influenzae
Гемофильная инфекция у детей младшего возраста протекает в виде бактериемии, гнойного менингита, пневмонии, целлюлита и эпиглоттита, у взрослых — в основном в виде пневмонии.
Тревогу ВОЗ вызывает развитие полной резистентности гемофильной палочки к ранее эффективному ампициллину, в результате чего от него пришлось повсеместно отказаться.
В России эффективны амоксициллин, цефалоспорины и макролиды, однако рекомендуется проводить бактериологический анализ с оценкой резистентности.
